电极电势思维导图
7、3、1、电极电势的产生 在一定条件下,当把金属放入含有该金属离子的盐溶液时,有两种反应倾向存在:一方面,金属表面的离子进入溶液和水分子结合成为水合离子,某种条件下达到平衡时金属表面带负电荷,靠近金属附近的溶液带正电荷,如图所示;另一方面,溶液中的水合离子有从金属表面获得电子,沉积到金属上的倾向,平衡
树图思维导图提供 电极电势 在线思维导图免费制作,点击“编辑”按钮,可对 电极电势 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:0e44e0966edc877baceb5894de148079
思维导图大纲
电极电势思维导图模板大纲
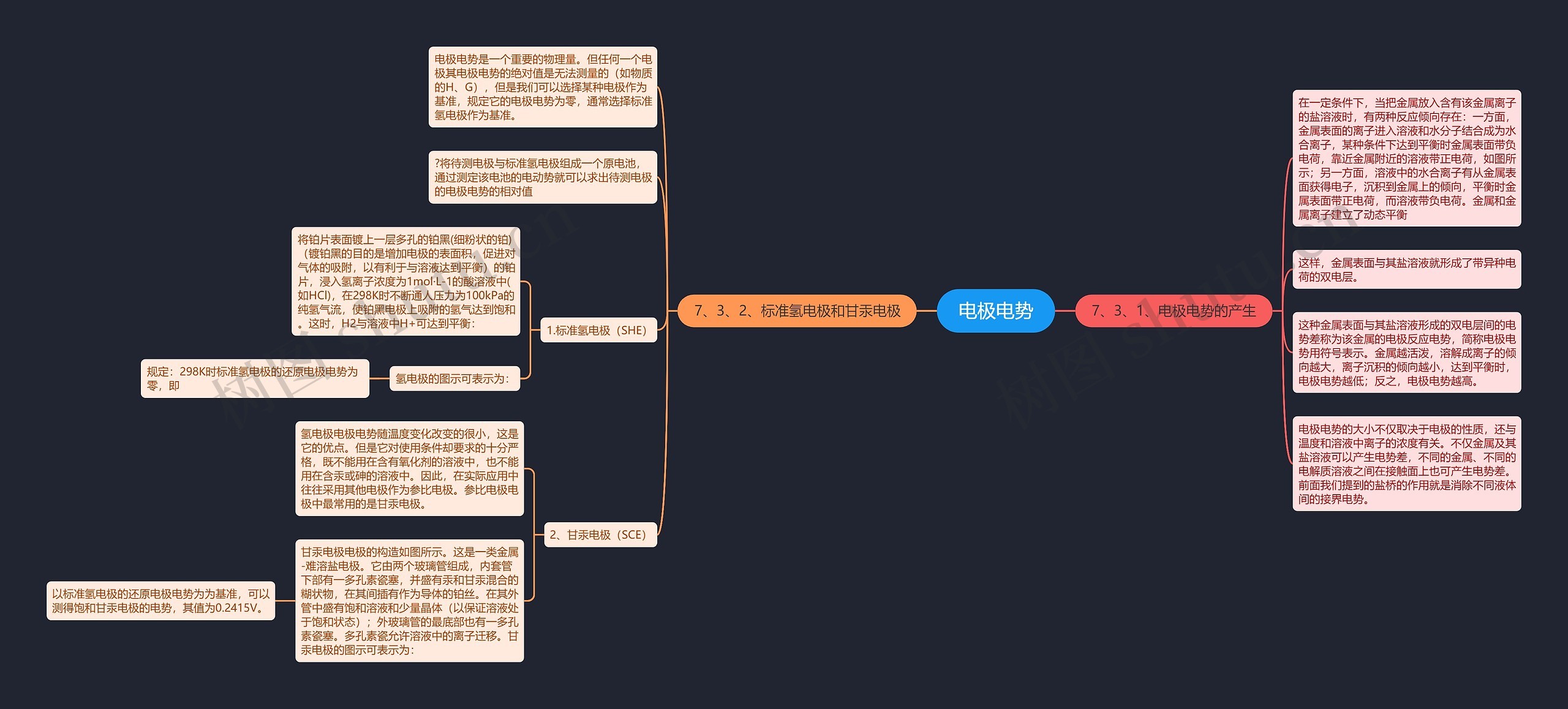
7、3、1、电极电势的产生
在一定条件下,当把金属放入含有该金属离子的盐溶液时,有两种反应倾向存在:一方面,金属表面的离子进入溶液和水分子结合成为水合离子,某种条件下达到平衡时金属表面带负电荷,靠近金属附近的溶液带正电荷,如图所示;另一方面,溶液中的水合离子有从金属表面获得电子,沉积到金属上的倾向,平衡时金属表面带正电荷,而溶液带负电荷。金属和金属离子建立了动态平衡
这样,金属表面与其盐溶液就形成了带异种电荷的双电层。
这种金属表面与其盐溶液形成的双电层间的电势差称为该金属的电极反应电势,简称电极电势用符号表示。金属越活泼,溶解成离子的倾向越大,离子沉积的倾向越小,达到平衡时,电极电势越低;反之,电极电势越高。
电极电势的大小不仅取决于电极的性质,还与温度和溶液中离子的浓度有关。不仅金属及其盐溶液可以产生电势差,不同的金属、不同的电解质溶液之间在接触面上也可产生电势差。前面我们提到的盐桥的作用就是消除不同液体间的接界电势。
7、3、2、标准氢电极和甘汞电极
电极电势是一个重要的物理量。但任何一个电极其电极电势的绝对值是无法测量的(如物质的H、G),但是我们可以选择某种电极作为基准,规定它的电极电势为零,通常选择标准氢电极作为基准。
?将待测电极与标准氢电极组成一个原电池,通过测定该电池的电动势就可以求出待测电极的电极电势的相对值
1.标准氢电极(SHE)
将铂片表面镀上一层多孔的铂黑(细粉状的铂)(镀铂黑的目的是增加电极的表面积,促进对气体的吸附,以有利于与溶液达到平衡)的铂片,浸入氢离子浓度为1mol·L-1的酸溶液中(如HCl),在298K时不断通人压力为100kPa的纯氢气流,使铂黑电极上吸附的氢气达到饱和。这时,H2与溶液中H+可达到平衡:
氢电极的图示可表示为:
规定:298K时标准氢电极的还原电极电势为零,即
2、甘汞电极(SCE)
氢电极电极电势随温度变化改变的很小,这是它的优点。但是它对使用条件却要求的十分严格,既不能用在含有氧化剂的溶液中,也不能用在含汞或砷的溶液中。因此,在实际应用中往往采用其他电极作为参比电极。参比电极电极中最常用的是甘汞电极。
甘汞电极电极的构造如图所示。这是一类金属-难溶盐电极。它由两个玻璃管组成,内套管下部有一多孔素瓷塞,并盛有汞和甘汞混合的糊状物,在其间插有作为导体的铂丝。在其外管中盛有饱和溶液和少量晶体(以保证溶液处于饱和状态);外玻璃管的最底部也有一多孔素瓷塞。多孔素瓷允许溶液中的离子迁移。甘汞电极的图示可表示为:
以标准氢电极的还原电极电势为为基准,可以测得饱和甘汞电极的电势,其值为0.2415V。
相关思维导图模板

树图思维导图提供 氧化还原反应脑图 在线思维导图免费制作,点击“编辑”按钮,可对 氧化还原反应脑图 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:ac7f3297282bc72829d56b3b4b60f556

树图思维导图提供 电极电势与氧化还原反应方向的关系 在线思维导图免费制作,点击“编辑”按钮,可对 电极电势与氧化还原反应方向的关系 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:e6ba7faf5eadefc3fed1019ea23f6271








 上海工商
上海工商