中华人民共和国药品管理法释义:第33条思维导图
核心内容:《中华人民共和国药品管理法》第33条应该怎样释义呢?药品管理法第33条规定的是对新药进行技术审评以及对已经批准生产的药品进行再评价管理。树图网编辑为您详细介绍关于药品管理法第33条的释义。
树图思维导图提供 中华人民共和国药品管理法释义:第33条 在线思维导图免费制作,点击“编辑”按钮,可对 中华人民共和国药品管理法释义:第33条 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:5611a4b4b8dc8a13dcd29aad3a352277
思维导图大纲
中华人民共和国药品管理法释义:第33条思维导图模板大纲
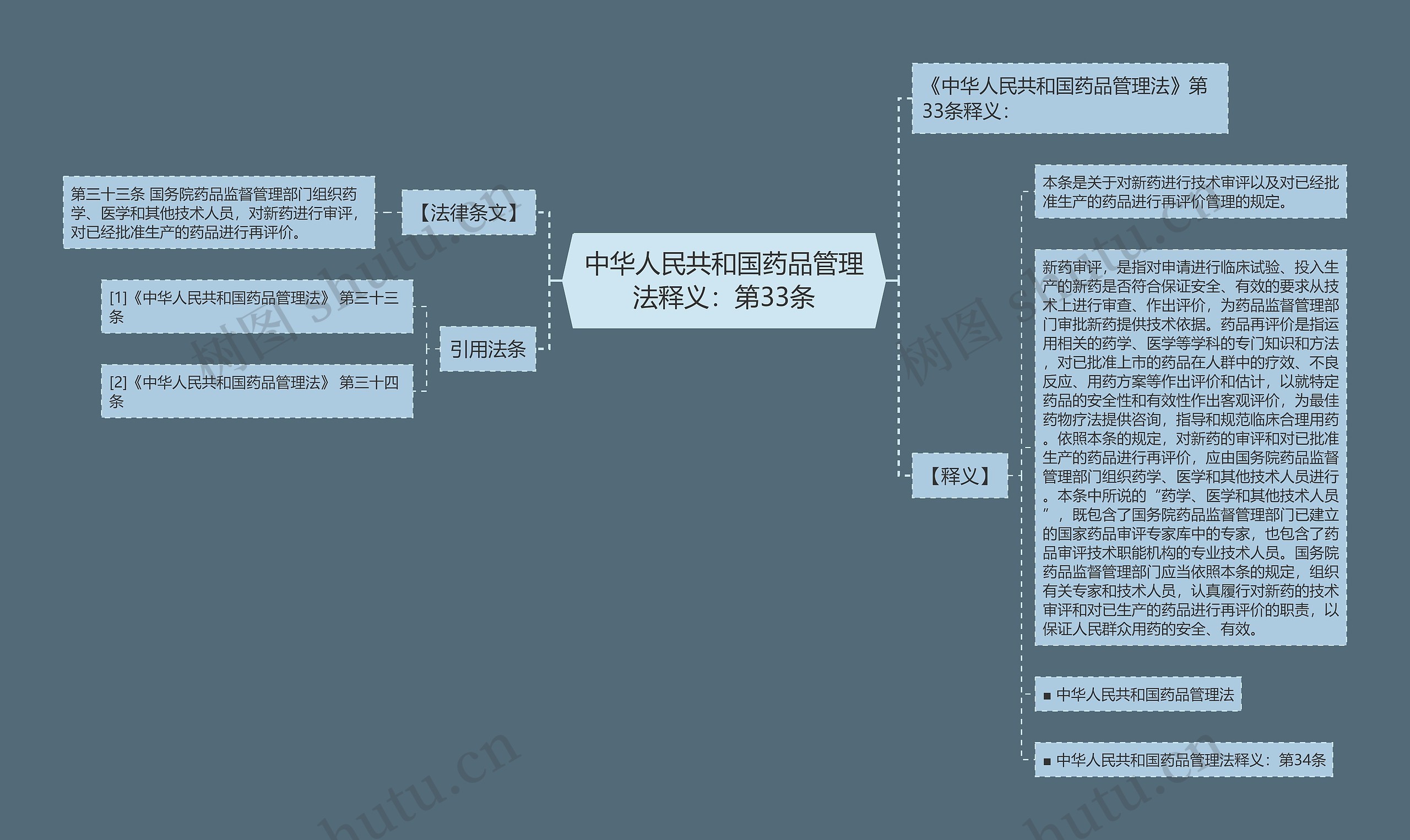
《中华人民共和国药品管理法》第33条释义:
【法律条文】
第三十三条 国务院药品监督管理部门组织药学、医学和其他技术人员,对新药进行审评,对已经批准生产的药品进行再评价。
【释义】
本条是关于对新药进行技术审评以及对已经批准生产的药品进行再评价管理的规定。
新药审评,是指对申请进行临床试验、投入生产的新药是否符合保证安全、有效的要求从技术上进行审查、作出评价,为药品监督管理部门审批新药提供技术依据。药品再评价是指运用相关的药学、医学等学科的专门知识和方法,对已批准上市的药品在人群中的疗效、不良反应、用药方案等作出评价和估计,以就特定药品的安全性和有效性作出客观评价,为最佳药物疗法提供咨询,指导和规范临床合理用药。依照本条的规定,对新药的审评和对已批准生产的药品进行再评价,应由国务院药品监督管理部门组织药学、医学和其他技术人员进行。本条中所说的“药学、医学和其他技术人员”,既包含了国务院药品监督管理部门已建立的国家药品审评专家库中的专家,也包含了药品审评技术职能机构的专业技术人员。国务院药品监督管理部门应当依照本条的规定,组织有关专家和技术人员,认真履行对新药的技术审评和对已生产的药品进行再评价的职责,以保证人民群众用药的安全、有效。
■ 中华人民共和国药品管理法
■ 中华人民共和国药品管理法释义:第34条
引用法条
[1]《中华人民共和国药品管理法》 第三十三条
[2]《中华人民共和国药品管理法》 第三十四条
相关思维导图模板


树图思维导图提供 904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查 在线思维导图免费制作,点击“编辑”按钮,可对 904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:10b9a8a2dd2fb4593f8130ef16c320fc

树图思维导图提供 第六章 群体传播与组织传播_副本 在线思维导图免费制作,点击“编辑”按钮,可对 第六章 群体传播与组织传播_副本 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:1672f555831e7d9a3bb2cf2fb792cb49







 上海工商
上海工商