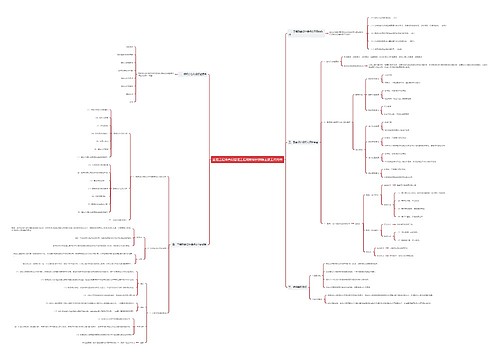
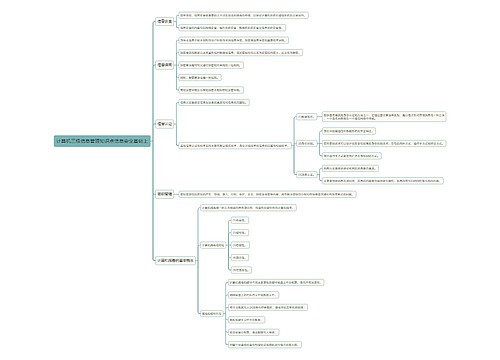
医疗器械说明书、标签和包装标识管理规定(征求意见稿)思维导图

核心内容:医疗器械说明书、标签和包装标识管理规定(征求意见稿)于2014年5月31日前向社会公开征求意见。医疗器械说明书、标签和包装标识管理规定(征求意见稿)全文共有二十六条,包括适用范围、医疗器械说明书、标签和包装标识的要求等内容。树图网编辑为您详细介绍。
树图思维导图提供 医疗器械说明书、标签和包装标识管理规定(征求意见稿) 在线思维导图免费制作,点击“编辑”按钮,可对 医疗器械说明书、标签和包装标识管理规定(征求意见稿) 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:cd744932911fbc956bd141bd42499828
思维导图大纲
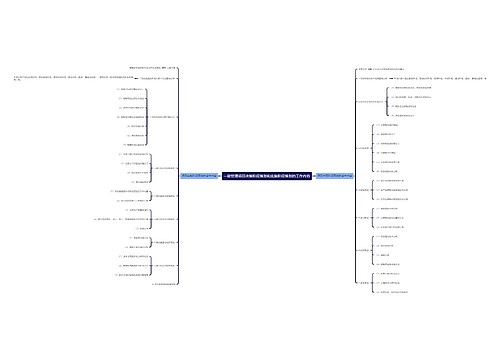
医疗器械说明书、标签和包装标识管理规定(征求意见稿)思维导图模板大纲
医疗器械说明书、标签和包装标识管理规定
(征求意见稿)
第一条为规范医疗器械说明书、标签和包装标识,保证医疗器械使用的安全,根据《医疗器械监督管理条例》,制定本规定。
第二条凡在中华人民共和国境内销售、使用的医疗器械应当按照本规定要求附有说明书、标签和包装标识。说明书、标签和包装标识中的某两项或者三项可以合并。
第三条医疗器械说明书是指由注册申请人或者备案人制作并随产品提供给用户的,能够涵盖该产品安全有效基本信息并用以指导正确安装、调试、操作、使用、维护、保养的技术文件。
医疗器械标签是指在医疗器械产品本体上附有的,用于识别产品特征和安全警示等信息的文字说明及图形、符号。
医疗器械包装标识是指在包装上标有的反映产品特征和安全警示等信息的文字说明及图形、符号。
第四条医疗器械的使用者应当按照说明书使用医疗器械。
第五条医疗器械说明书、标签和包装标识的内容应当真实、完整、准确、科学,并与产品特性相一致。医疗器械标签、包装标识的内容应当与说明书有关内容相符合。
第六条医疗器械说明书、标签和包装标识对疾病名称、专业名词、诊断治疗过程和结果的表述,应当采用国家统一颁布或者规范的专用词汇,度量衡单位应当符合国家标准的规定。
第七条医疗器械说明书、标签和包装标识中使用的符号或者识别颜色应当符合国家相关标准的规定。无相关标准规定的,该符号及识别颜色应当在说明书中描述。
第八条医疗器械的产品名称应当清晰地标明在说明书、标签和包装标识的显著位置,并与医疗器械注册证或者备案信息表中的产品名称一致。
第九条医疗器械说明书、标签和包装标识文字内容应当使用中文,可以附加其他文种。中文的使用应当符合国家通用的语言文字规范。
医疗器械说明书、标签和包装标识中的文字、符号、表格、数字、图形等应当准确、清晰、规范。
第十条医疗器械最小销售单元必须附有说明书。
第十一条医疗器械说明书应当符合国家标准或者行业标准有关要求,一般应当包括以下内容:
(一)通用名称、型号、规格;
(二)注册申请人或者备案人名称、注册地址、联系方式及售后服务单位,进口医疗器械还应当载明医疗器械的代理人的名称、地址、联系方式;
(三)生产企业的名称和地址、许可证编号或者生产备案号;(四)医疗器械注册号或者备案号;
(五)产品技术要求的编号;
(六)产品性能、主要结构组成或者成分、预期用途;
(七)禁忌症、注意事项、警示以及提示的内容;
(八)安装和使用说明或者图示,由消费者个人自行使用的医疗器械还应当具有安全使用的特别说明;
(九)产品维护和保养方法,特殊储存、运输条件、方法;
(十)限期使用的产品,应当标明有效期限;
(十一)配件清单,对配件的规格型号等及附属品、损耗品、配件的更换周期以及更换的方法进行说明;
(十二)医疗器械标签所用的图形、符号、缩写等内容的解释;
(十三)说明书的编制或者修订日期及版本号。
第十二条医疗器械说明书中有关注意事项、警示以及提示性内容主要包括:
(一)产品使用的对象;
(二)潜在的安全危害及使用限制;
(三)产品在正确使用过程中出现意外时,对操作者、使用者的保护措施以及应当采取的应急和纠正措施;
(四)必要的控制监测评估手段、特殊人群;
(五)一次性使用产品应当注明“一次性使用”字样或者符号,已灭菌产品应当注明灭菌方式以及灭菌包装损坏后的处理方法,使用前需要消毒或者灭菌的应当说明消毒或者灭菌的方法;
(六)产品需要同其他医疗器械产品一起安装或者联合使用时,应当注明联合使用器械的要求、使用方法、注意事项;
(七)在使用过程中,与其他产品可能产生的相互干扰及其可能出现的危害;
(八)产品使用中可能带来的不良事件或者产品成份中含有的可能引进副作用的成份或者辅料;
(九)有关器械丢弃时应当注意的事项,产品使用后需要处理的,应当注明相应的处理方法;
(十)根据产品特性,应当提示操作者、使用者注意的其他事项。
第十四条医疗器械标签、包装标识一般应当包括以下内容:
(一)通用名称、型号、规格;
(二)注册申请人或者备案人名称、注册地址、生产地址、联系方式,进口医疗器械还应当载明医疗器械的代理人的名称、地址、联系方式;
(三)医疗器械注册号或者备案号;
(四)生产企业的名称、许可证编号或者生产备案号;
(五)生产日期或者批(编)号,对于限期使用的产品,应当标明有效日期或者失效日期;
(六)电源连接条件、输入功率;
(七)根据产品特性应当标注的图形、符号以及其他相关内容;
(八)必要的警告、注意事项;
(九)特殊储存、操作条件或者说明。
第十五条医疗器械包装标识还应当有贮藏条件、运输注意事项以及产品用后必要的处理方式。
第十六条医疗器械标签和包装标识因位置或者大小受限而无法全部标明上述内容的,至少应当标注产品名称、型号规格、生产日期或者批(编)号、有效日期或者失效日期,并在标签和包装标识中明确“其他内容详见说明书”。
第十七条使用中对环境有破坏或者负面影响的医疗器械,其标签应当注明影响环境的物质及其对环境的作用(如使用氟利昂对臭氧层的破坏)。对使用后的废弃物的处理应当予明示。
第十八条带放射或者辐射的医疗器械,其标签应当包含警示标志或者中文警示说明,标明辐射的性质、种类、强度及分布情形及操作注意事项。
第十九条医疗器械说明书、标签和包装标识不得有下列内容:
(一)含有“疗效最佳”、“保证治愈”、“包治”、“根治”、“即刻见效”、“完全无毒副作用”等表示功效的断言或者保证的;
(二)含有“最高技术”、“最科学”、“最先进”、“最佳”等绝对化语言和表示的;
(三)说明治愈率或者有效率的;
(四)与其他企业产品的功效和安全性相比较的;
(五)含有“保险公司保险”、“无效退款”等承诺性语言的;
(六)利用任何单位或者个人的名义、形象作证明或者推荐的;
(七)含有误导性说明,使人感到已经患某种疾病,或者使人误解不使用该医疗器械会患某种疾病或者加重病情的表述的;
(八)法律、法规规定禁止的其他内容。
第二十条器械说明书应当由注册申请人或者备案人在申请医疗器械注册或者办理备案时,按照《医疗器械注册与备案管理办法》的规定提交食品药品监督管理部门审查或者备案,提交的说明书内容应当与其他注册或者备案资料相符合。
第二十一条注册申请人变更经注册审查的医疗器械说明书内容,应当向医疗器械注册的原审批部门书面告知,并提交说明书更改情况对比说明等相关文件。说明书变更内容涉及到《医疗器械注册与备案管理办法》规定应当办理注册变更情形的,按相应规定办理。
第二十二条原注册审批部门自收到注册申请人更改说明书的书面告知之日起,在20个工作日内未发出有不同意见的书面通知的,说明书更改生效,并由原注册审批部门予以备案;在20个工作日内发出书面通知的,注册申请人应当按照通知要求办理。
第二十三条备案人更改已备案的说明书,不涉及《医疗器械注册与备案管理办法》规定应当办理变更备案信息情形的,应当按照质量管理体系的相关要求进行记录;涉及需办理变更备案情形的,应当办理变更备案。
第二十四条违反本规定,有下列情形之一的,由县级以上食品药品监督管理部门按照《医疗器械监督管理条例》第六十七条的规定予以处罚:
(一)擅自更改经注册审查的说明书的内容的;
(二)上市产品的标签、包装标识与经注册审查的说明书内容相违背,或者违反本规定其他要求的;
(三)上市产品未按规定附说明书、标签和包装标识的。
第二十五条医疗器械注册申请人擅自在医疗器械说明书中增加产品适用范围或者适应症、预期用途的,由食品药品监督管理部门依照《医疗器械监督管理条例》有关未取得医疗器械注册证书的情形予以处罚。
第二十六条本规定自2014年×月×日起实施。
引用法条
[1]《医疗器械监督管理条例》 第二条
[2]《医疗器械监督管理条例》 第三条
[3]《医疗器械监督管理条例》 第四条
[4]《医疗器械监督管理条例》 第五条
[5]《医疗器械监督管理条例》 第六条
[6]《医疗器械监督管理条例》 第七条
[7]《医疗器械监督管理条例》 第八条
[8]《医疗器械监督管理条例》 第九条
[9]《医疗器械监督管理条例》
[10]《医疗器械监督管理条例》
[11]《医疗器械监督管理条例》
[12]《医疗器械监督管理条例》
[13]《医疗器械监督管理条例》
[14]《医疗器械监督管理条例》
[15]《医疗器械监督管理条例》
[16]《医疗器械监督管理条例》
[17]《医疗器械监督管理条例》
[18]《医疗器械监督管理条例》
[19]《医疗器械监督管理条例》 第二十条
[20]《医疗器械监督管理条例》 第六十七条
[21]《医疗器械监督管理条例》 第二十五条
[22]《医疗器械监督管理条例》 第二十六条
相关思维导图模板

树图思维导图提供 9.战斗的基督教 在线思维导图免费制作,点击“编辑”按钮,可对 9.战斗的基督教 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:33d168acd0cd9f767f809c7a5df86e3a

树图思维导图提供 数智技术在工程设备管理中的应用 在线思维导图免费制作,点击“编辑”按钮,可对 数智技术在工程设备管理中的应用 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:f9a2de84ad9a9ceebc96385d71be9ebe




 上海工商
上海工商