化学必修一知识点整理思维导图
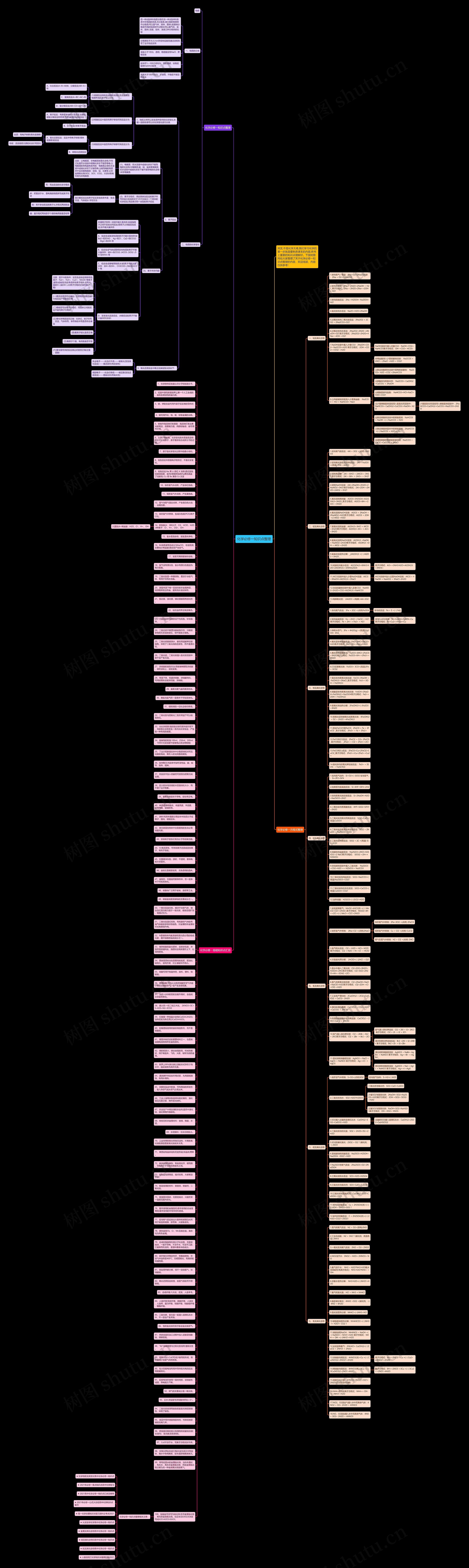
其实,不是化学太难,我们学习化学的第一步就是要熟悉课本的内容,将书上重要的知识点理解好。
树图思维导图提供 化学必修一知识点整理 在线思维导图免费制作,点击“编辑”按钮,可对 化学必修一知识点整理 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:30710e781b8a7163878119f01162d2d4
思维导图大纲
化学必修一知识点整理思维导图模板大纲
其实,不是化学太难,我们学习化学的第一步就是要熟悉课本的内容,将书上重要的知识点理解好。下面树图网给大家整理了关于化学必修一知识点整理的内容,欢迎阅读,内容仅供参考!
化学必修一知识点整理
物质
一、物质的分类
把一种(或多种)物质分散在另一种(或多种)物质中所得到的体系,叫分散系.被分散的物质称作分散质(可以是气体、液体、固体),起容纳分散质作用的物质称作分散剂(可以是气体、液体、固体).溶液、胶体、浊液三种分散系的比较
分散质粒子大小/nm外观特征能否通过滤纸有否丁达尔效应实例
溶液小于1均匀、透明、稳定能没有NaCl、蔗糖溶液
胶体在1—100之间均匀、有的透明、较稳定能有Fe(OH)3胶体
浊液大于100不均匀、不透明、不稳定不能没有泥水
二、物质的化学变化
1、物质之间可以发生各种各样的化学变化,依据一定的标准可以对化学变化进行分类.
(1)根据反应物和生成物的类别以及反应前后物质种类的多少可以分为:
A、化合反应(A+B=AB)B、分解反应(AB=A+B)
C、置换反应(A+BC=AC+B)
D、复分解反应(AB+CD=AD+CB)
(2)根据反应中是否有离子参加可将反应分为:
A、离子反应:有离子参加的一类反应.主要包括复分解反应和有离子参加的氧化还原反应.
B、分子反应(非离子反应)
(3)根据反应中是否有电子转移可将反应分为:
A、氧化还原反应:反应中有电子转移(得失或偏移)的反应
实质:有电子转移(得失或偏移)
特征:反应前后元素的化合价有变化
B、非氧化还原反应
2、离子反应
(1)、电解质:在水溶液中或熔化状态下能导电的化合物,叫电解质.酸、碱、盐都是电解质.在水溶液中或熔化状态下都不能导电的化合物,叫非电解质.
注意:①电解质、非电解质都是化合物,不同之处是在水溶液中或融化状态下能否导电.②电解质的导电是有条件的:电解质必须在水溶液中或熔化状态下才能导电.③能导电的物质并不全部是电解质:如铜、铝、石墨等.④非金属氧化物(SO2、SO3、CO2)、大部分的有机物为非电解质.
(2)、离子方程式:用实际参加反应的离子符号来表示反应的式子.它不仅表示一个具体的化学反应,而且表示同一类型的离子反应.
复分解反应这类离子反应发生的条件是:生成沉淀、气体或水.书写方法:
写:写出反应的化学方程式
拆:把易溶于水、易电离的物质拆写成离子形式
删:将不参加反应的离子从方程式两端删去
查:查方程式两端原子个数和电荷数是否相等
(3)、离子共存问题
所谓离子在同一溶液中能大量共存,就是指离子之间不发生任何反应;若离子之间能发生反应,则不能大量共存.
A、结合生成难溶物质的离子不能大量共存:如Ba2+和SO42-、Ag+和Cl-、Ca2+和CO32-、Mg2+和OH-等
B、结合生成气体或易挥发性物质的离子不能大量共存:如H+和CO32-,HCO3-,SO32-,OH-和NH4+等
C、结合生成难电离物质(水)的离子不能大量共存:如H+和OH-、CH3COO-,OH-和HCO3-等.
D、发生氧化还原反应、水解反应的离子不能大量共存(待学)
注意:题干中的条件:如无色溶液应排除有色离子:Fe2+、Fe3+、Cu2+、MnO4-等离子,酸性(或碱性)则应考虑所给离子组外,还有大量的H+(或OH-).(4)离子方程式正误判断(六看)
(一)看反应是否符合事实:主要看反应能否进行或反应产物是否正确
(二)看能否写出离子方程式:纯固体之间的反应不能写离子方程式
(三)看化学用语是否正确:化学式、离子符号、沉淀、气体符号、等号等的书写是否符合事实
(四)看离子配比是否正确
(五)看原子个数、电荷数是否守恒
(六)看与量有关的反应表达式是否正确(过量、适量)
3、氧化还原反应中概念及其相互关系如下:
失去电子——化合价升高——被氧化(发生氧化反应)——是还原剂(有还原性)
得到电子——化合价降低——被还原(发生还原反应)——是氧化剂(有氧化性)
化学必修一方程式整理
一、钠及其化合物
1.钠与氧气:常温:4Na+O2=2Na2O点燃:2Na + O2=(△)Na2O2
2.钠与水反应:2Na + 2H2O=2NaOH + H2↑_离子方程式:2Na + 2H2O=2Na++2OH-+ H2↑
3.钠与硫酸反应:2Na +H2SO4= Na2SO4+H2↑
4.氧化钠与水反应:Na2O+H2O=2NaOH
5.过氧化钠与二氧化碳反应:2Na2O2 + 2CO2 = 2Na2CO3+O2↑
6.过氧化钠与水反应:2Na2O2+2H2O =4NaOH+O2↑离子方程式:2Na2O2+2H2O=4Na++4OH-+O2↑
7.NaOH溶液中通入少量CO2:2NaOH+CO2= Na2CO3+H2O 离子方程式:2OH-+CO2= CO32-+H2O
NaOH溶液中通入过量CO2:NaOH+CO2= NaHCO3离子方程式:OH-+CO2= HCO3-
8.①向碳酸钠溶液滴入少量稀盐酸: Na2CO3 + HCl = NaHCO3+ NaCl
向稀盐酸滴入少量碳酸钠溶液: Na2CO3 + 2HCl = 2NaCl +H2O + CO2↑
②除去碳酸氢钠溶液中混有的碳酸钠: Na2CO3+ H2O +CO2 =2NaHCO3
③碳酸钠与氢氧化钙: Na2CO3+ Ca(OH)2 =CaCO3↓ + 2NaOH
④碳酸氢钠与盐酸: NaHCO3+HCl=NaCl+H2O+CO2↑
⑤少量碳酸氢钠溶液滴入氢氧化钙溶液中: NaHCO3+ Ca(OH)2=CaCO3↓+NaOH+ H2O
少量氢氧化钙溶液滴入碳酸氢钠溶液中:2NaHCO3+Ca(OH)2=CaCO3↓+Na2CO3+2H2O
⑥除去碳酸钠溶液中的碳酸氢钠:NaHCO3 + NaOH =(△) Na2CO3 + H2O
⑦除去碳酸钠固体中的碳酸氢钠:2NaHCO3 =(△) Na2CO3 + H2O+CO2 ↑
⑧鉴别碳酸钠和碳酸氢钠溶液:Na2CO3 + CaCl2 =CaCO3↓ + 2NaCl
二、铝及其化合物
1.铝与氧气的反应:4Al + 3O2 =(点燃) 2Al2O3
2.铝与氧化铁反应(铝热反应):2Al + Fe2O3 =(高温) 2Fe + Al2O3
3.铝和稀盐酸:2Al + 6HCl = 2AlCl3 + 3H2↑ 离子方程式:2Al + 6H+ = 2Al3+ + 3H2↑
4.铝和NaOH溶液:2Al+2NaOH+2H2O=2NaAlO2+3H2↑离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑
5.氧化铝和稀硫酸:Al2O3+3H2SO4=Al2(SO4)3+3H2O_离子方程式:Al2O3+6H+=2Al3++3H2O
6.氧化铝和NaOH溶液:Al2O3 + 2NaOH = 2NaAlO2+H2O离子方程式:Al2O3 + 2OH-=2 AlO2-+H2O
7.氢氧化铝和盐酸:Al(OH)3+3HCl = AlCl3+3H2O离子方程式:Al(OH)3+3H+ = Al3++3H2O
8.氢氧化铝和NaOH溶液:Al(OH)3 +NaOH = NaAlO2+2H2O离子方程式:Al(OH)3 +OH-= AlO2-+2H2O
9.氢氧化铝受热分解:_2Al(OH)3 =(△) Al2O3 +3H2O _
10.硫酸铝与氨水反应:Al2(SO4)3+6NH3·H2O=2Al(OH)3↓+3(NH4)2SO4
离子方程式:Al3++3NH3·H2O=Al(OH)3↓+3NH4+
11.AlCl3溶液中加入少量NaOH溶液:AlCl3+3NaOH=Al(OH)3↓+3NaCl
AlCl3溶液中加入过量NaOH溶液:AlCl3 + 4NaOH = NaAlO2 + 3NaCl+2H2O
12.往偏铝酸钠溶液中通入足量CO2:NaAlO2+2H2O+CO2=Al(OH)3↓+NaHCO3
13.电解氧化铝: 2Al2O3 =(电解) 4Al+3O2↑
三、铁及其化合物
1.铁与氧气反应:3Fe + 2O2 =(点燃)Fe3O4
铁与硫反应:Fe + S =(△) FeS
2.铁与盐酸反应:Fe + 2HCl = FeCl2 + H2↑离子方程式:Fe + 2H+ = Fe2+ + H2↑
铁与CuSO4溶液:Fe+CuSO4=FeSO4+Cu离子方程式:Fe+Cu2+=Fe2++Cu
3.铁和水蒸气:3Fe + 4H2O(g) =(高温) Fe3O4+ 4H2_
4.氧化亚铁与盐酸反应:FeO+2HCl=FeCl2+H2O离子方程式:FeO+2H+=Fe2++H2O
5.氧化铁与盐酸反应:Fe2O3+6HCl=2FeCl3+3H2O离子方程式:Fe2O3+6H+=2Fe3++3H2O
6.CO还原氧化铁:Fe2O3+ 3CO=(高温)2Fe + 3CO2
7.氯化铁与氢氧化钠溶液:FeCl3+3NaOH = Fe(OH)3↓+3NaCl_离子方程式:Fe3++3OH-= Fe(OH)3↓
8.硫酸亚铁与氢氧化钠溶液:FeSO4+2NaOH=Fe(OH)2↓+Na2SO4离子方程式:Fe2++2OH-= Fe(OH)2↓
9.氢氧化铁加热分解:2Fe(OH)3=(△)Fe2O3+3H2O
10.氢氧化亚铁被氧化成氢氧化铁:4Fe(OH)2 + O2 + 2H2O =4Fe(OH)3
11.除去FeCl2中的FeCl3:2FeCl3 + Fe = 3FeCl2 _离子方程式:2Fe3+ + Fe = 3Fe2+
12.FeCl2和Cl2反应:2FeCl2 + Cl2= 2FeCl3_离子方程式:_2Fe2+ + Cl2 = 2Fe3++2Cl-
13.FeCl3和Cu反应:2FeCl3+Cu=2FeCl2+CuCl2_离子方程式:2Fe3++Cu=2Fe2++Cu2+
14.氯化铁与硫氰化钾溶液反应: Fe3+ + 3SCN- = Fe(SCN)3
四、硅及其化合物
1.硅与氧气加热:Si+O2=(△)SiO2 硅与氟气:Si+2F2=SiF4
2.硅单质与氢氟酸反应:Si+4HF=SiF4+2H2
3.硅与氢氧化钠溶液反应:Si+2NaOH+H2O=Na2SiO3+2H2↑
4.二氧化硅与氢氟酸反应:4HF+SiO2=SiF4↑+2H2O
5.二氧化硅与氧化钙高温反应:SiO2+CaO=(高温)CaSiO3
6.二氧化硅与氢氧化钠溶液反应:SiO2 + 2NaOH = Na2SiO3+ H2O
7.二氧化硅与碳反应:SiO2 + 2C =(高温) Si + 2CO↑
8.硅酸钠与盐酸反应:Na2SiO3+2HCl=H2SiO3↓+2 NaCl离子方程式: SiO32-+2H+=H2SiO3↓
9.往硅酸钠溶液中通入二氧化碳: Na2SiO3 +CO2+H2O == H2SiO3↓+ Na2CO3
10.二氧化硅与纯碱反应:SiO2+Na2CO3=(高温)Na2SiO3+CO2↑
11.二氧化硅与石灰石反应:SiO2+CaCO3=(高温)CaSiO3+CO2↑
12.加热硅酸:H2SiO3=(△)SiO2+H2O
五、氯及其化合物
1.实验室制氯气:MnO2+4HCl(浓) =(△) MnCl2+Cl2↑+2H2O_离子方程式:MnO2+4H++2Cl-=(△) Mn2++Cl2↑+2H2O
2.钠在氯气中燃烧: 2Na+Cl2 =(点燃)2NaCl
铁在氯气中燃烧:2Fe+3Cl2 =(点燃) 2FeCl3
铜在氯气中燃烧:Cu + Cl2 =(点燃) CuCl2
氢气在氯气中燃烧:H2 + Cl2 =(点燃) 2HCl
3.氯气和水反应:Cl2 + H2O = HCl+ HClO 离子方程式:Cl2 + H2O = H++Cl- + HClO
4.次氯酸光照分解: 2HClO=(△)2HCl + O2↑
5.氯水中通入二氧化硫:Cl2+SO2+2H2O=H2SO4+2HCl离子方程式:Cl2+SO2+2H2O=4H++SO42-+2Cl-
6.氯气与氢氧化钠溶液:Cl2+2NaOH=NaCl+NaClO+H2O离子方程式:Cl2+2OH-=Cl-+ClO-+H2O
7.工业生产漂白粉:2Ca(OH)2 + 2Cl2=Ca(ClO)2 + CaCl2+ 2H2O
8.漂白粉漂白原理:Ca(ClO)2 + CO2+ H2O =CaCO3↓ + 2HClO
9.向漂白粉溶液中加入稀盐酸:Ca(ClO)2 + 2HCl=CaCl2 + 2HClO
10.氯气通入溴化钾溶液:Cl2 + 2KBr = Br2+ 2KCl离子方程式:Cl2 + 2Br- = Br2 + 2Cl-
氯气通入碘化钾溶液:Cl2 + 2KI = I2+ 2KCl 离子方程式:Cl2 + 2I- = I2 + 2Cl-
溴水和碘化钾溶液反应:Br2 +2KI = I2+2KBr 离子方程式:Br2 +2I- = I2+2Br-
11.氯化钠和硝酸银溶液:AgNO3 + NaCl = AgCl↓ + NaNO3 离子方程式:Ag++Cl- = AgCl↓
溴化钠和硝酸银溶液:AgNO3 + NaBr= AgBr↓ + NaNO3 离子方程式:Ag++Br- = AgBr↓_
碘化钠和硝酸银溶液:AgNO3 + NaI = AgI↓ + NaNO3 离子方程式:Ag++I-=AgI↓
六、硫及其化合物
1.硫在空气中燃烧:S+O2=(点燃)SO2
硫与氢气加热:S+H2=(△)H2S
2.二氧化硫与水:SO2+H2O?H2SO3
二氧化硫与氧化钙:SO2+CaO=CaSO3
少量SO2与氢氧化钠:2NaOH+SO2=Na2SO3+H2O离子方程式:2OH-+SO2= SO32-+H2O
过量SO2与氢氧化钠:NaOH+SO2=NaHSO3离子方程式:OH-+SO2= HSO3-
3.SO2通入过量的澄清石灰水:Ca(OH)2+SO2=CaSO3↓+H2O
过量的SO2通入澄清石灰水:Ca(OH)2+2SO2=Ca(HSO3)2
4.二氧化硫与硫化氢:SO2 + 2H2S=3S↓+2H2O
5.SO2的催化氧化:2SO2 + O2 ? (催化剂、△) 2SO3
6.亚硫酸钠和硫酸反应:Na2SO3+H2SO4=Na2SO4 +SO2↑+H2O
7.Na2SO3与氧气反应:2Na2SO3+O2=2Na2SO4
8.三氧化硫和水反应:SO3+H2O=H2SO4
9.三氧化硫与氧化钙:SO3+CaO= CaSO4
10.三氧化硫与氢氧化钙:Ca(OH)2+SO3=CaSO4↓+H2O
11.铜与浓硫酸反应:Cu + 2H2SO4(浓)=(△)CuSO4 + 2H2O+SO2 ↑
12.碳与浓硫酸反应:C + 2H2SO4(浓)=(△) 2H2O+CO2↑+2SO2↑
七、氮及其化合物
1.氮气和氧气反应:N2 + O2=(放电)2NO
2.工业合成氨:N2 + 3H2 ? (催化剂、高温高压) 2NH3
3.一氧化氮与氧气反应:2NO + O2= 2NO2
4.NO2溶于水:3NO2 + H2O= 2HNO3+ NO
5.氨气溶于水: NH3 + H2O?NH3·H2O氨水显弱碱性(电离方程式):NH3·H2O?NH4+ + OH-
6.浓氨水受热分解: NH3·H2O=(△)NH3↑+H2O
7.氨气和氯化氢:HCl + NH3 = NH4Cl
8.氨的催化氧化:4NH3 +5O2 =(催化剂、△) 4NO + 6H2O
9.氯化铵受热分解:NH4Cl=(△)NH3+HCl
10.碳酸氢铵受热分解:NH4HCO3 =(△)NH3 ↑+ H2O↑+ CO2 ↑
11.硝酸铵和NaOH:NH4NO3 + NaOH =(△) NaNO3 + NH3↑+H2O 离子方程式:NH4++ OH-=(△)NH3↑+H2O
12.实验室制氨气:2NH4Cl+ Ca(OH)2=(△)CaCl2 + 2NH3↑ + 2H2O
13.浓硝酸与铜反应:4HNO3(浓)+Cu =(△) Cu(NO3)2+2NO2↑+2H2O
离子方程式:4H++2NO3-+Cu =(△) Cu2++2NO2↑+2H2O
14.稀硝酸与铜反应:8HNO3(稀)+3Cu =(△) 3Cu(NO3)2+2NO↑+4H2O
离子方程式:8H++2NO3-+3Cu =(△) 3Cu2++2NO↑+4H2O
15.硝酸见光分解:4HNO3=4NO2↑+O2↑+2H2O(见光或受热分解)
16.NH4+的检验离子方程式:NH4++ OH-=(△)NH3↑+H2O
17.NO2、O2混合气通入水中无剩余气体:4NO2 + O2+ 2H2O = 4HNO3
18.NO、O2混合通入水中无剩余气体:4NO + 3O2+ 2H2O = 4HNO3
化学必修一易错知识点汇总
1、化学的特征就是认识分子和制造分子。
2、结晶牛胰岛素是世界上第一个人工合成的,具有生理活性的蛋白质。
3、钠、钾的合金可用作原子反应堆的导热剂。
4、钠可用作钛、锆、铌、钽等金属的冶炼。
5、钠制作高压钠灯的原因:高压钠灯发出黄光射程远,透雾能力强,肉眼较敏感,故可用作灯塔。
6、从原子角度看,化学变化的本质是反应物的分子分成原子,原子重新组合成新分子的过程。
7、原子是化学变化过程中的最小微粒。
8、焰色反应本质是电子的跃迁,不是化学变化。
9、焰色反应:Na 黄 Li 紫红 K 浅紫(透过蓝色钴玻璃观察,因为K里面常混有Na黄色掩盖了浅紫色) Cu 绿 Ba 黄绿 Co 淡蓝
10、铁在氯气中点燃,产生棕红色烟。
11、铜在氯气中点燃,产生黄色烟。
12、氯气与氢气混合点燃,产生苍白色火焰,出现白雾。
13、磷在氯气中燃烧,生成白色烟(PCl5)雾(PCl3)。
14、新制氯水:3种分子:Cl2、HClO、H2O;4种离子:Cl-、H+、ClO-、OH-
久置氯水=稀盐酸:H2O、Cl-、H+、OH-
15、氯水是混合物,液氯是纯净物。
16、84消毒液有效成分为NaClO,与洁厕灵(主要成分稀盐酸)混合后产生氯气。
17、液氯可用钢罐储存运输。
18、氯气没有漂白性,氯水有漂白性是因为有次氯酸。
19、二氧化氯是一种黄绿色、易溶于水的气体,常用于饮用水消毒。
20、溴是常温下唯一呈液态的非金属单质,液溴易挥发且有毒,通常用水液封保存。
21、氯化银,溴化银,碘化银都具有感光性。
22、硅在自然界没有游离态。
23、三氧化硫在标准状况下为无色、针状晶体。
24、二氧化硫不能漂白酸碱指示剂,只能使紫色的石蕊溶液变红,但不能使之褪色。
25、二氧化硫能使溴水、酸性高锰酸钾溶液褪色,体现了二氧化硫的还原性,而不是漂白性。
26、二氧化硫,二氧化碳通入氯化钡溶液中都不会产生沉淀。
27、浓硫酸的鉴别方法:用玻璃棒蘸取浓硫酸,滴在滤纸上,滤纸变黑。
28、常温下铁、铝遇浓硫酸、浓硝酸钝化,可用铝槽车运输浓硫酸、浓硝酸。
29、臭氧与氧气是同素异形体。
30、臭氧与氧气在一定条件下可相互转化。
31、硒和碲的一切化合物均有毒。
32、二氧化氮与四氧化二氮在常温下可以相互转化。
33、光化学烟雾:氮的氧化物在紫外线作用下,与碳氢化合物发生一系列光化学反应,产生的一种有毒的烟雾。
34、容量瓶的规格:100ml、250ml、500ml、1000ml(实验题中容量瓶必须注明规格)
35、丁达尔现象是胶体中分散质微粒对可见光散射而成,需在入射光侧面观察到。
36、胶体聚沉:向胶体中加可溶性盐、酸、碱等、加热、搅拌。
37、向豆浆中加入硫酸钙可使蛋白质聚沉成豆腐。
38、区分胶体与溶液的本质是微粒大小,而不是丁达尔现象。
39、氢氧化铁胶体不带电,胶粒带正电。
40、半透膜:动物肠衣、鸡蛋壳膜、羊皮膜、胶棉薄膜、玻璃纸等。
41、渗析:利用半透膜分离胶体中杂质分子或离子,提纯、精制胶体。
42、铁元素是生物体中含量最高的生命必需微量元素。
43、亚铁离子使血红蛋白分子有载氧功能。
44、Vc有还原性,可将铁离子还原成亚铁离子,有利于吸收。
45、石墨是深灰色,质软,不透明,易导电的片状固体。
46、金刚石是硬度极高,无色透明的晶体。
47、金刚石、石墨是同素异形体,在一定条件下可相互转化。
48、碳酸钠广泛用于玻璃,造纸等工业。
49、碳酸氢钠是发酵粉的主要成分之一。
50、一氧化氮是无色,难溶于水的气体,结合血红蛋白能力强于一氧化碳,能使血管扩张,增强记忆力。
51、二氧化氮是红棕色,有刺激性气味的有毒气体能使多种织物褪色,对金属和非金属材料也有腐蚀作用。
52、N是植物体内氨基酸和蛋白质必需的组成元素,是叶绿素的组成成分之一。
53、储存碳酸氢氨化肥时,应密封包装,并放在阴凉通风处,施肥时应将其埋在土下,以保持肥效。
54、尿素是目前含氮量最高的氮肥,肥效比较持久,使用方便,对土壤破坏作用小。
55、硝酸可用于制造炸药、染料、塑料、硝酸盐。
56、发烟硝酸:95%以上的浓硝酸在空气中由于挥发出硝酸蒸气,会产生发烟现象。
57、当进入水体的氮的含量升高时,会造成水体富营养化。
58、黑火药:一硫二硝三木炭。 2KNO3+3C+S=K2S+N2+3CO2
59、石膏是一种结晶水合物(CaSO4·2H2O);加热后变为熟石膏(2CaSO4·H2O)。
60、钡餐透视使用硫酸钡做造影剂,而不是碳酸钡。
61、锂是热核反应的重要材料之一,也是制造锂电池和特种合金的原料。
62、镁的密度小,镁合金强度高,机械性能好,用于制造车,飞机,火箭,被称为国防金属。
63、世界上99%溴元素以溴的形式存在于海水中,因此被称为海洋元素。
64、清洗碘升华实验所用试管,先用酒精清洗,再用水清洗。
65、溶解在苦卤中的溴,可利用溴的挥发性,鼓入热空气或水蒸气分离出来。
66、工业上溴用来制造燃料的抗爆剂,溴化银见光易分解,用作感光材料。
67、农业生产中用含溴的杀虫剂;医药中溴化钠,溴化钾用作镇静剂。
68、传统无机非金属材料:玻璃,陶瓷,水泥。
69、水泥原料:石灰石和黏土。
70、工业常用氢氧化钙做沉淀剂,不用氢氧化钠的原因是氢氧化钠成本太高。
71、单质硅有晶体硅和无定形硅(非晶体)两种。
72、晶体硅是灰黑色,有金属光泽,硬而脆,导电性介于导体和绝缘体之间。
73、硅酸盐性质稳定,熔点较高,大都难溶于水。
74、制造玻璃的材料:碳酸钠,碳酸钙,二氧化硅。
75、玻璃是非晶体,无固定熔点,只能在某一温度范围内软化。
76、最早使用的金属是铜;最早使用的合金是青铜;最早使用的半导体材料是锗。
77、铝与氧气反应放出大量热和耀眼白光可用于制造燃烧弹、信号弹、火箭推进剂。
78、黑色金属:Fe、Cr、Mn及其合金。其余均为有色金属。
79、合成树脂是有机高分子化合物,无固定熔点,一般不导电,不溶于水,可溶于乙醇,乙醚等有机溶剂,是塑料最基本的成分。
80、碳纤维化学稳定性好,耐酸碱腐蚀,在空气中加热至400℃,无明显氧化,有良好的低温性能。
81、铵盐受热都分解,但不一定放氨气,如硝酸铵。
82、氧化还原反应较慢,故氯气吸收可不防倒吸。
83、合成纤维:六大纶、尼龙、人造羊毛。
84、人造纤维:黏胶纤维,醋酸纤维,人造丝,人造棉,蛋白纤维,硝酸纤维,硝酸酯纤维,醋酸纤维。
85、二氧化碳、氯化氢一起通入澄清石灰水中,不一定会产生浑浊。
86、饱和氯化钠可用于除去氯化铁蒸气。
87、肉类食品在加工过程中加入适量亚硝酸钠,保鲜防腐。
88、"84"消毒原理与过氧化氢相同:强氧化性。
89、燃煤中加入CaO可减少酸雨的形成,但不能减少温室气体的排放。
90、硅太阳能电池利用半导体的光电效应实现能量转化。
91、铅蓄电池在使用一段时间后,溶液酸性减弱,导电能力下降。
92、煤气的主要成分是一氧化碳。
93、王水:浓盐酸与浓硝酸体积比=3:1。
94、二氧化硫使滴有酚酞的氢氧化钠溶液褪色,体现了酸性。
95、食品中用木糖醇做甜味剂,可降低糖尿病的犯病几率。
96、焊接废旧钢材前分别用饱和碳酸钠溶液(去油污),氯化氨溶液(除锈)。
97、CuS不溶于水,写离子方程式时不拆。
98、河海交界处形成三角洲:因为泥沙中有胶体,海水中有电解质,胶体遇到电解质聚沉。
99、带有结晶水的金属氧化物,加热失重时,先失水,再失非金属氧化物,然后金属氧化物分解为另一种金属氧化物放氧气。
100、硅酸盐可改写为氧化物:先写金属氧化物,再写非金属氧化物。如正长石KAlSi3O8改写成K2O·Al2O3·6SiO2。
化学必修一知识点整理相关文章:
★ 化学物质及其变化高中化学必修一知识点
★ 2021年必修一重点知识点高中化学复习
★ 2021高中化学必修一知识点口诀及解释
★ 2021年必修一公式大总结高中化学知识点复习
★ 高一化学主要知识点复习资料必考点2021
★ 从实验学化学高中化学必修一知识点
★ 金属及其化合物高中化学必修一知识点
★ 硅及其化合物Si高中化学必修一知识点
★ 硫及其化合物高中化学必修一知识点
★ 人教版高三化学知识点整理归纳2021










 上海工商
上海工商