药品GMP认证主要过程思维导图

药品GMP认证主要过程: 1.认证申请和资料审查申请单位须向所在省、自治区、直辖市药品监督管理部门报送药品gmp认证申请书“及《药品gmp认证管理办法》中规定的有关资料。
树图思维导图提供 药品GMP认证主要过程 在线思维导图免费制作,点击“编辑”按钮,可对 药品GMP认证主要过程 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:9598477339b80c7e266cbad4d6779f98
思维导图大纲
药品GMP认证主要过程思维导图模板大纲
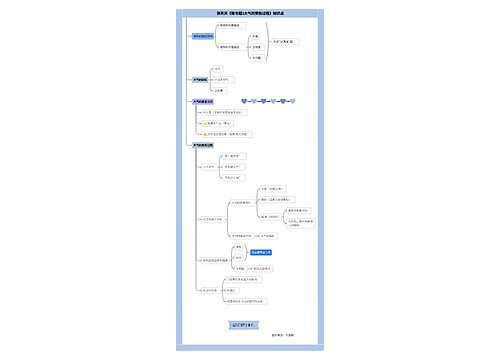
药品GMP认证主要过程:
1.认证申请和资料审查申请单位须向所在省、自治区、直辖市药品监督管理部门报送药品gmp认证申请书“及《药品gmp认证管理办法》中规定的有关资料。省、自治区、直辖市药品监督管理部门在收到材料之日起的20个工作日内,对申请材料进行初审,并将初审意见及申请材料报送国家药品监督管理局安全监管司,经安全监管司受理、形式审查后,转交国家药品监督管理局药品认证管理中心(以下简称”局认证中心“)。局认证中心在接到申请资料后的20个工作日内对申请资料进行技术审查,提出审查意见,并书面通知申请单位。
2.制定现场检查方案对通过资料审查的单位制定现场检查方案,并在资料审查通过之日起的20个工作日内组织现场检查。
3.现场检查局认证中心负责组织gmp认证现场检查。现场检查组由国家药品监督管理局药品gmp检查员组成,现场检查实行组长负责制,检查组将检查结果形成检查报告上报局认证中心。
4.检查报告的审核局认证中心在接到检查组提交的现场检查报告及相关资料之日起的20个工作日内,提出审核意见,送国家药品监督管理局安全监管司。
5.认证批准经国家药品监督管理局安全监管司审核后报局领导审批。国家药品监督管理局在收到局认证中心审核意见之日起20个工作日内,作出是否批准的决定。对审批结果为“合格”的药品生产企业(车间),由国家药品监督管理局颁发“药品gmp证书”,并予以公告。
“药品gmp证书”的有效期为5年。新开办的药品生产企业(车间)的“药品gmp证书”有效期为1年。











 上海工商
上海工商