补充申请的申报|审批方法思维导图

补充申请的申报|审批方法: 第一百一十条 变更研制新药、生产药品和进口药品已获批准证明文件及其附件中载明事项的,应当提出补充申请。 申请人应当参照相关技术指导原则,评估其变更对药品安全性、有效性和质量可控性的影响,并进行相应的技术研究工作。
树图思维导图提供 补充申请的申报|审批方法 在线思维导图免费制作,点击“编辑”按钮,可对 补充申请的申报|审批方法 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:ea8e4e92da57f5b7b44a2439da1e9747
思维导图大纲
补充申请的申报|审批方法思维导图模板大纲
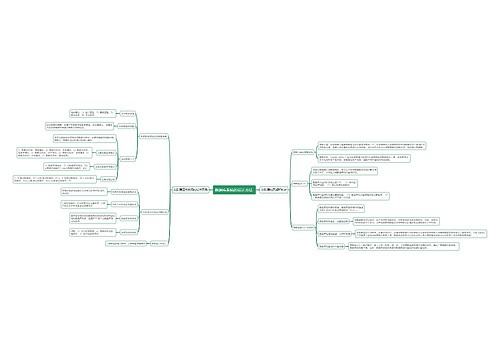
补充申请的申报|审批方法:
第一百一十条 变更研制新药、生产药品和进口药品已获批准证明文件及其附件中载明事项的,应当提出补充申请。
申请人应当参照相关技术指导原则,评估其变更对药品安全性、有效性和质量可控性的影响,并进行相应的技术研究工作。
第一百一十一条 申请人应当填写《药品补充申请表》,向所在地省、自治区、直辖市药品监督管理部门报送有关资料和说明。省、自治区、直辖市药品监督管理部门对申报资料进行形式审查,符合要求的,出具药品注册申请受理通知书;不符合要求的,出具药品注册申请不予受理通知书,并说明理由。
第一百一十二条 进口药品的补充申请,申请人应当向国家食品药品监督管理局报送有关资料和说明,提交生产国家或者地区药品管理机构批准变更的文件。国家食品药品监督管理局对申报资料进行形式审查,符合要求的,出具药品注册申请受理通知书;不符合要求的,出具药品注册申请不予受理通知书,并说明理由。
第一百一十三条 修改药品注册标准、变更药品处方中已有药用要求的辅料、改变影响药品质量的生产工艺等的补充申请,由省、自治区、直辖市药品监督管理部门提出审核意见后,报送国家食品药品监督管理局审批,同时通知申请人。
相关思维导图模板

树图思维导图提供 抓住重点 在线思维导图免费制作,点击“编辑”按钮,可对 抓住重点 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:4c49e4799ddf94a339c56e46eb96a826

树图思维导图提供 农村幼儿园利用绘本阅读开展安全教育的实践研究_副本 在线思维导图免费制作,点击“编辑”按钮,可对 农村幼儿园利用绘本阅读开展安全教育的实践研究_副本 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:2000927dcd222b18fa95af52d1709af8









 上海工商
上海工商