初中化学金属必考知识点整理思维导图
有很多的学生在复习化学时,因为之前都没对知识进行一下总结,导致我们在复习时整体效率低下。
树图思维导图提供 初中化学金属必考知识点整理 在线思维导图免费制作,点击“编辑”按钮,可对 初中化学金属必考知识点整理 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:35f8b774b8e05ef808f98aadafbebe79
思维导图大纲
初中化学金属必考知识点整理思维导图模板大纲
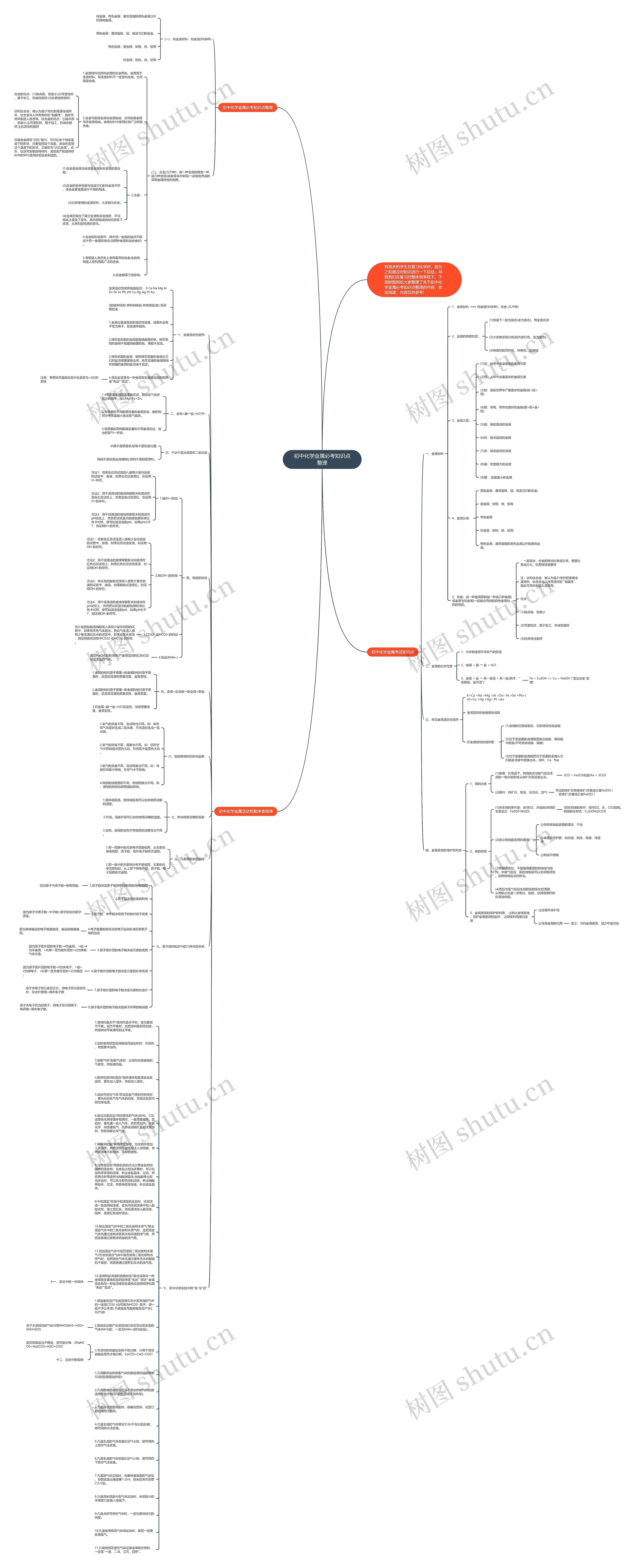
有很多的学生在复习化学时,因为之前都没对知识进行一下总结,导致我们在复习时整体效率低下。下面树图网给大家整理了关于初中化学金属必考知识点整理的内容,欢迎阅读,内容仅供参考!
初中化学金属必考知识点整理
(一)、纯金属材料:纯金属(90多种)
纯金属:有色金属:通常是指除黑色金属以外的其他金属。
黑色金属:通常指铁、锰、铬及它们的合金。
有色金属:重金属:如铜、锌、铅等
轻金属:如钠、镁、铝等
(二)、合金(几千种):由一种金属跟其他一种或几种金属(或金属与非金属)一起熔合而成的具有金属特性的物质。
1.金属材料包括纯金属和合金两类。金属属于金属材料,但金属材料不一定是纯金属,也可能是合金。
2.合金可能是金属与金属组成,也可能是金属与非金属组成。金属材料中使用比较广泛的是合金。
合金的优点:(1)熔点高、密度小;(2)可塑性好、易于加工、机械性能好;(3)抗腐蚀性能好;
钛和钛合金:被认为是21世纪的重要金属材料,钛合金与人体有很好的"相容性",因此可用来制造人造骨等。钛合金的优点:①熔点高、密度小;②可塑性好、易于加工、机械性能好;③抗腐蚀性能好
钛镍合金具有"记忆"能力,可记住某个特定温度下的形状,只要复回这个温度,就会恢复到这个温度下的形状,又被称为"记忆金属"。此外,钛还可制取超导材料,美国生产的超导材料中的90%是用钛铌合金制造的。
3.注意:
(1)合金是金属与金属或金属与非金属的混合物。
(2)合金的很多性能与组成它们的纯金属不同,使合金更容易适于不同的用途。
(3)日常使用的金属材料,大多数为合金。
(4)金属在熔合了其它金属和非金属后,不仅组成上发生了变化,其内部组成结构也发生了改变,从而引起性质的变化。
4.合金的形成条件:其中任一金属的熔点不能高于另一金属的沸点(当两种金属形成合金时)。
5.青铜是人类历史上使用最早的合金;生铁和钢是人类利用最广泛的合金.
6.合金都属于混合物。
初中化学金属考试知识点
一、金属材料
1、金属材料
纯金属(90多种),合金 (几千种)
2、金属的物理性质:
(1)常温下一般为固态(汞为液态),有金属光泽。
(2)大多数呈银白色(铜为紫红色,金为黄色)
(3)有良好的导热性、导电性、延展性
3、金属之最:
(1)铝:地壳中含量最多的金属元素
(2)钙:人体中含量最多的金属元素
(3)铁:目前世界年产量最多的金属(铁>铝>铜)
(4)银:导电、导热性最好的金属(银>铜>金>铝)
(5)铬:硬度最高的金属
(6)钨:熔点最高的金属
(7)汞:熔点最低的金属
(8)锇:密度最大的金属
(9)锂 :密度最小的金属
4、金属分类:
黑色金属:通常指铁、锰、铬及它们的合金。
重金属:如铜、锌、铅等
有色金属
轻金属:如钠、镁、铝等;
有色金属:通常是指除黑色金属以外的其他金属。
5、合金:由一种金属跟其他一种或几种金属(或金属与非金属)一起熔合而成的具有金属特性的物质。
:一般说来,合金的熔点比各成分低,硬度比各成分大,抗腐蚀性能更好
注:钛和钛合金:被认为是21世纪的重要金属材料,钛合金与人体有很好的`"相容性",因此可用来制造人造骨等。
优点
(1)熔点高、密度小
(2)可塑性好、易于加工、机械性能好
(3)抗腐蚀性能好
二、金属的化学性质
1、大多数金属可与氧气的反应
2、金属 + 酸 → 盐 + H2↑
3、金属 + 盐 → 另一金属 + 另一盐(条件:"前换后,盐可溶")
Fe + CuSO4 == Cu + FeSO4 ("湿法冶金"原理)
三、常见金属活动性顺序
K>Ca >Na >Mg >Al >Zn> Fe >Sn >Pb>(H)>Cu >Hg >Ag> Pt >Au
金属活动性由强逐渐减弱
在金属活动性顺序里:
(1)金属的位置越靠前,它的活动性就越强
(2)位于氢前面的金属能置换出盐酸、稀硫酸中的氢(不可用浓硫酸、硝酸)
(3)位于前面的金属能把位于后面的金属从它们的盐溶液中置换出来。(除K、Ca、Na)
四、金属资源的保护和利用
1、铁的冶炼
(1)原理:在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来。
3CO + Fe2O3高温2Fe + 3CO2
(2)原料:铁矿石、焦炭、石灰石、空气
常见的铁矿石有磁铁矿(主要成分是Fe3O4 )、赤铁矿(主要成分是Fe2O3 )
2、铁的锈蚀
(1)铁生锈的条件是:铁与O2、水接触(铁锈的主要成分:Fe2O3·XH2O)
(铜生铜绿的条件:铜与O2、水、CO2接触。铜绿的化学式:Cu2(OH)2CO3)
(2)防止铁制品生锈的措施:
①保持铁制品表面的清洁、干燥
②表面涂保护膜:如涂油、刷漆、电镀、烤蓝等
③制成不锈钢
(3)铁锈很疏松,不能阻碍里层的铁继续与氧气、水蒸气反应,因此铁制品可以全部被锈蚀。因而铁锈应及时除去。
(4)而铝与氧气反应生成致密的氧化铝薄膜,从而阻止铝进一步氧化,因此,铝具有很好的抗腐蚀性能。
3、金属资源的保护和利用: ①防止金属腐蚀,保护金属资源的途径: ②回收利用废旧金属
③合理开采矿物
④寻找金属的代用
意义:节约金属资源,减少环境污染
初中化学金属活动性顺序表规律
一、金属活动性顺序:
金属活动性顺序由强至弱: K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
(按顺序背诵) 钾钙钠镁铝 锌铁锡铅(氢) 铜汞银铂金
1.金属位置越靠前的活动性越强,越易失去电子变为离子,反应速率越快。
2.排在氢前面的金属能置换酸里的氢,排在氢后的金属不能置换酸里的氢,跟酸不反应。
3.排在前面的金属,能把排在后面的金属从它们的盐溶液里置换出来。排在后面的金属跟排在前面的金属的盐溶液不反应。
4.混合盐溶液与一种金属发生置换反应的顺序是"先远""后近"。
注意:单质铁在置换反应中总是变为+2价的亚铁
二、金属+酸→盐+H2↑中:
1.4等质量金属跟足量酸反应,放出氢气由多至少的顺序:Al>Mg>Fe>Zn。
2.等质量的不同酸跟足量的金属反应,酸的相对分子质量越小放出氢气越多。
3.等质量的同种酸跟足量的不同金属反应,放出的氢气一样多。
三、干冰不是冰是固态二氧化碳
水银不是银是汞;铅笔不是铅是石墨;
纯碱不是碱是盐(碳酸钠);塑钢不是钢是塑料。
四、物质的检验
1.酸(H+)检验
方法1:将紫色石蕊试液滴入盛有少量待测液的试管中,振荡,如果石蕊试液变红,则证明H+存在。
方法2:用干燥清洁的玻璃棒蘸取未知液滴在蓝色石蕊试纸上,如果蓝色试纸变红,则证明H+的存在。
方法3:用干燥清洁的玻璃棒蘸取未知液滴在pH试纸上,然后把试纸显示的颜色跟标准比色卡对照,便可知道溶液的pH,如果pH小于7,则证明H+的存在。
2.碱(OH-)的检验
方法1:将紫色石蕊试液滴入盛有少量待测液的试管中,振荡,如果石蕊试液变蓝,则证明OH-的存在。
方法2:用干燥清洁的玻璃棒蘸取未知液滴在红色石蕊试纸上,如果红色石蕊试纸变蓝,则证明OH-的存在。
方法3:将无色的酚酞试液滴入盛有少量待测液的试管中,振荡,如果酚酞试液变红,则证明OH-的存在。
方法4:用干燥清洁的玻璃棒蘸取未知液滴在pH试纸上,然后把试纸显示的颜色跟标准比色卡对照,便可知道溶液的pH,如果pH大于7,则证明OH-的存在。
3.CO32- 或HCO3-的检验
将少量的盐酸或硝酸倒入盛有少量待测物的试管中,如果有无色气体放出,将此气体通入盛有少量澄清石灰水的试管中,如果石灰水变浑,则证明原待测物中CO32-或HCO3-的存在。
4.铵盐(NH4+)
用浓NaOH溶液(微热)产生使湿润的红色石蕊试纸变蓝的气体。
五、金属+盐溶液→新金属+新盐:
1.金属的相对原子质量>新金属的相对原子质量时,反应后溶液的质量变重,金属变轻。
2.金属的相对原子质量<新金属的相对原子质量时,反应后溶液的质量变轻,金属变重。
3.在金属+酸→盐+H2↑反应后,溶液质量变重,金属变轻。
六、物质燃烧时的影响因素:
1.氧气的浓度不同,生成物也不同。如:碳在氧气充足时生成二氧化碳,不充足时生成一氧化碳。
2.氧气的浓度不同,现象也不同。如:硫在空气中燃烧是淡蓝色火焰,在纯氧中是蓝色火焰。
3.氧气的浓度不同,反应程度也不同。如:铁能在纯氧中燃烧,在空气中不燃烧。
4.物质的接触面积不同,燃烧程度也不同。如:煤球的燃烧与蜂窝煤的燃烧。
七、影响物质溶解的因素:
1.搅拌或振荡。搅拌或振荡可以加快物质溶解的速度。
2.升温。温度升高可以加快物质溶解的速度。
3.溶剂。选用的溶剂不同物质的溶解性也不同。
八、元素周期表的规律:
1.同一周期中的元素电子层数相同,从左至右核电荷数、质子数、核外电子数依次递增。
2.同一族中的元素核外电子数相同、元素的化学性质相似,从上至下核电荷数、质子数、电子层数依次递增。
九、原子结构知识中的八种决定关系:
1.质子数决定原子核所带的电荷数(核电荷数)
因为原子中质子数=核电荷数。
2.质子数决定元素的种类
3.质子数、中子数决定原子的相对原子质量
因为原子中质子数+中子数=原子的相对原子质量。
4.电子能量的高低决定电子运动区域距离原子核的远近
因为离核越近的电子能量越低,越远的能量越高。
5.原子最外层的电子数决定元素的类别
因为原子最外层的电子数<4为金属,>或=4为非金属,=8(第一层为最外层时=2)为稀有气体元素。
6.原子最外层的电子数决定元素的化学性质
因为原子最外层的电子数<4为失电子,>或=4为得电子,=8(第一层为最外层时=2)为稳定。
7.原子最外层的电子数决定元素的化合价
原子失电子后元素显正价,得电子后元素显负价,化合价数值=得失电子数
8.原子最外层的电子数决定离子所带的电荷数
原子失电子后为阳离子,得电子后为阴离子,电荷数=得失电子数。
十、初中化学实验中的"先"与"后"
1.使用托盘天平?使用托盘天平时,首先要调节平衡。调节平衡时,先把游码移到零刻度,然后转动平衡螺母到达平衡。
2.加热使用试管或烧瓶给药品加热时,先预热,然后集中加热。
3.制取气体?制取气体时,必须先检查装置的气密性,然后装药品。
4.固体和液体的混合?固体液体相互混合或反应时,要先加入固体,然后加入液体。
5.试验可燃性气体?在试验氢气等的可燃性时,要先检验氢气等气体的纯度,然后试验其可燃性等性质。
6.氧化还原反应?用还原性的气体(如H2、CO)还原氧化铜等固体物质时,一般需要加热。实验时,要先通一会儿气体,然后再加热。实验完毕,继续通氢气,先移去酒精灯直到试管冷却,然后再移去导气管。
7.稀释浓硫酸?稀释浓硫酸时,先往烧杯里加入蒸馏水,然后沿烧杯壁慢慢注入浓硫酸,并用玻璃棒不断搅拌,冷却后装瓶。
8.分离混合物?用重结晶的方法分离食盐和硝酸钾的混合物,当食盐占相当多量时,可以先加热蒸发饱和溶液,析出食盐晶体,过滤,然后再冷却母液析出硝酸钾晶体;当硝酸钾占相当多量时,可以先冷却热饱和溶液,析出硝酸钾晶体,过滤,然后再蒸发母液,析出食盐晶体。
9.中和滴定?在做中和滴定的实验时,待测溶液一般选用碱溶液,应先向待测溶液中加入酚酞试剂,使之显红色,然后逐滴加入酸溶液,搅拌,直至红色恰好退去。
10.除去混合气体中的二氧化碳和水蒸气?除去混合气体中的二氧化碳和水蒸气时,应把混合气体先通过盛有浓氢氧化钠溶液的洗气瓶,然后接着通过盛有浓硫酸的洗气瓶。
11.检验混合气体中是否混有二氧化碳和水蒸气?在检验混合气体中是否混有二氧化碳和水蒸气时,应把混合气体先通过盛有无水硫酸铜的干燥管,然后再通过盛有石灰水的洗气瓶。
12.金属和盐溶液的置换反应?混合溶液与一种金属发生置换反应的顺序是"先远""后近";金属混合物与一种盐溶液发生置换反应的顺序也是"先远""后近"。
十一、反应中的一些规律:
1.跟盐酸反应产生能澄清石灰水变浑浊的气体的一定是CO32-(也可能为HCO3- 离子,但一般不予以考虑) 凡碳酸盐与酸都能反应产生CO2气体
2.跟碱反应能产生使湿润红色石蕊试纸变蓝的气体(NH3)的,一定为NH4+(即为铵盐)。
溶于水显碱性的气体只有NH3(NH3+H2O=NH3·H2O)
3.可溶性的碳酸盐加热不能分解,只有不溶性碳酸盐受热才能分解。CaCO3=CaO+CO2↑
酸式碳酸盐也不稳定,受热易分解:2NaHCO3=Na2CO3+H2O+CO2↑
十二、实验中的规律:
1.凡用固体加热制取气体的都选用高锰酸钾制O2装置(固固加热型);
2.凡用固体与液体反应且不需加热制气体的都选用双氧水制O2装置(固液不加热型)。
3.凡是给试管固体加热,都要先预热,试管口都应略向下倾斜。
4.凡是生成的气体难溶于水(不与水反应)的,都可用排水法收集。
5.凡是生成的气体密度比空气大的,都可用向上排空气法收集。
6.凡是生成的气体密度比空气小的,都可用向下排空气法收集。
7.凡是制气体实验时,先要检查装置的气密性,导管应露出橡皮塞1-2ml,铁夹应夹在距管口1/3处。
8.凡是用长颈漏斗制气体实验时,长颈漏斗的末端管口应插入液面下。
9.凡是点燃可燃性气体时,一定先要检验它的纯度。
10.凡是使用有毒气体做实验时,最后一定要处理尾气。
11.凡是使用还原性气体还原金属氧化物时,一定是"一通、二点、三灭、四停"。
相关思维导图模板


树图思维导图提供 2024年8月--2023年8月时政整合 在线思维导图免费制作,点击“编辑”按钮,可对 2024年8月--2023年8月时政整合 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:8212d18ea45f416edca4ef534194fc99


树图思维导图提供 卫生化学--元素和无机物分析 在线思维导图免费制作,点击“编辑”按钮,可对 卫生化学--元素和无机物分析 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:4c942d0350c858e06a1f7ed29a86d096





 上海工商
上海工商