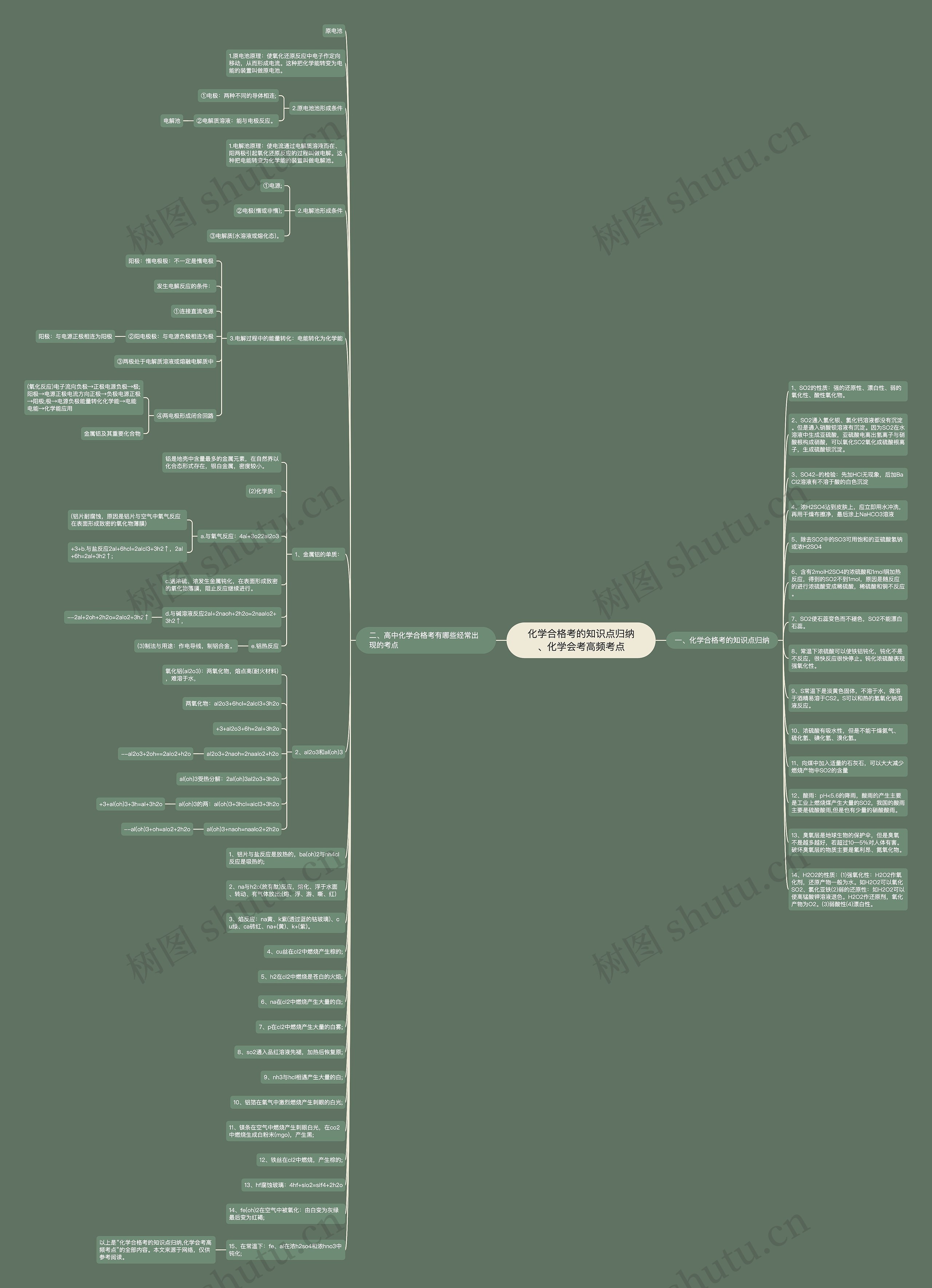
化学合格考的知识点归纳、化学会考高频考点思维导图
关于“化学合格考的知识点归纳,化学会考高频考点”,小编从网络整理了以下化学合格考的知识点归纳,化学会考高频考点,一起来看下吧。了解更多内容微信搜索关注公众号:“壹壹考生网”,关注了解更多
树图思维导图提供 化学合格考的知识点归纳、化学会考高频考点 在线思维导图免费制作,点击“编辑”按钮,可对 化学合格考的知识点归纳、化学会考高频考点 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:53d83ba4a2f7690cc2b8ceb2d341f840
思维导图大纲
化学合格考的知识点归纳、化学会考高频考点思维导图模板大纲
一、化学合格考的知识点归纳
1、SO2的性质:强的还原性、漂白性、弱的氧化性、酸性氧化物。
2、SO2通入氯化钡、氯化钙溶液都没有沉淀。但是通入硝酸钡溶液有沉淀。因为SO2在水溶液中生成亚硫酸,亚硫酸电离出氢离子与硝酸根构成硝酸,可以氧化SO2氧化成硫酸根离子,生成硫酸钡沉淀。
3、SO42-的检验:先加HCl无现象,后加BaCl2溶液有不溶于酸的白色沉淀
4、浓H2SO4沾到皮肤上,应立即用水冲洗,再用干燥布擦净,最后涂上NaHCO3溶液
5、除去SO2中的SO3可用饱和的亚硫酸氢钠或浓H2SO4
6、含有2molH2SO4的浓硫酸和1mol铜加热反应,得到的SO2不到1mol,原因是随反应的进行浓硫酸变成稀硫酸,稀硫酸和铜不反应。
7、SO2使石蕊变色而不褪色,SO2不能漂白石蕊。
8、常温下浓硫酸可以使铁铝钝化,钝化不是不反应,很快反应很快停止。钝化浓硫酸表现强氧化性。
9、S常温下是淡黄色固体,不溶于水,微溶于酒精易溶于CS2。S可以和热的氢氧化钠溶液反应。
10、浓硫酸有吸水性,但是不能干燥氨气、硫化氢、碘化氢、溴化氢。
11、向煤中加入适量的石灰石,可以大大减少燃烧产物中SO2的含量
12、酸雨:pH<5.6的降雨,酸雨的产生主要是工业上燃烧煤产生大量的SO2,我国的酸雨主要是硫酸酸雨,但是也有少量的硝酸酸雨。
13、臭氧层是地球生物的保护伞,但是臭氧不是越多越好,若超过10—5%对人体有害。破坏臭氧层的物质主要是氟利昂、氮氧化物。
14、H2O2的性质:(1)强氧化性:H2O2作氧化剂,还原产物一般为水。如H2O2可以氧化SO2、氯化亚铁(2)弱的还原性:如H2O2可以使高锰酸钾溶液退色。H2O2作还原剂,氧化产物为O2。(3)弱酸性(4)漂白性。
二、高中化学合格考有哪些经常出现的考点
原电池
1.原电池原理:使氧化还原反应中电子作定向移动,从而形成电流。这种把化学能转变为电能的装置叫做原电池。
2.原电池池形成条件
①电极:两种不同的导体相连;
②电解质溶液:能与电极反应。
电解池
1.电解池原理:使电流通过电解质溶液而在、阳两极引起氧化还原反应的过程叫做电解。这种把电能转变为化学能的装置叫做电解池。
2.电解池形成条件
①电源;
②电极(惰或非惰);
③电解质(水溶液或熔化态)。
3.电解过程中的能量转化:电能转化为化学能
阳极:惰电极极:不一定是惰电极
发生电解反应的条件:
①连接直流电源
②阳电极极:与电源负极相连为极
阳极:与电源正极相连为阳极
③两极处于电解质溶液或熔融电解质中
④两电极形成闭合回路
(氧化反应)电子流向负极→正极电源负极→极;阳极→电源正极电流方向正极→负极电源正极→阳极;极→电源负极能量转化化学能→电能电能→化学能应用
金属铝及其重要化合物
1、金属铝的单质:
铝是地壳中含量最多的金属元素,在自然界以化合态形式存在,银白金属,密度较小。
(2)化学质:
a.与氧气反应:4al+3o22al2o3
(铝片耐腐蚀,原因是铝片与空气中氧气反应在表面形成致密的氧化物薄膜)
+3+b.与盐反应2al+6hcl=2alcl3+3h2↑,2al+6h=2al+3h2↑;
c.遇浓硫、浓发生金属钝化,在表面形成致密的氧化物薄膜,阻止反应继续进行。
d.与碱溶液反应2al+2naoh+2h2o=2naalo2+3h2↑,
--2al+2oh+2h2o=2alo2+3h2↑
e.铝热反应
(3)制法与用途:作电导线,制铝合金。
2、al2o3和al(oh)3
氧化铝(al2o3):两氧化物,熔点高(耐火材料),难溶于水,
两氧化物:al2o3+6hcl=2alcl3+3h2o
+3+al2o3+6h=2al+3h2o
al2o3+2naoh=2naalo2+h2o
--al2o3+2oh==2alo2+h2o
al(oh)3受热分解:2al(oh)3al2o3+3h2o
al(oh)3的两:al(oh)3+3hcl=alcl3+3h2o
+3+al(oh)3+3h=al+3h2o
al(oh)3+naoh=naalo2+2h2o
--al(oh)3+oh=alo2+2h2o
1、铝片与盐反应是放热的,ba(oh)2与nh4cl反应是吸热的;
2、na与h2o(放有酞)反应,熔化、浮于水面、转动、有气体放出;(熔、浮、游、嘶、红)
3、焰反应:na黄、k紫(透过蓝的钴玻璃)、cu绿、ca砖红、na+(黄)、k+(紫)。
4、cu丝在cl2中燃烧产生棕的;
5、h2在cl2中燃烧是苍白的火焰;
6、na在cl2中燃烧产生大量的白;
7、p在cl2中燃烧产生大量的白雾;
8、so2通入品红溶液先褪,加热后恢复原;
9、nh3与hcl相遇产生大量的白;
10、铝箔在氧气中激烈燃烧产生刺眼的白光;
11、镁条在空气中燃烧产生刺眼白光,在co2中燃烧生成白粉末(mgo),产生黑;
12、铁丝在cl2中燃烧,产生棕的;
13、hf腐蚀玻璃:4hf+sio2=sif4+2h2o
14、fe(oh)2在空气中被氧化:由白变为灰绿最后变为红褐;
15、在常温下:fe、al在浓h2so4和浓hno3中钝化;
以上是“化学合格考的知识点归纳,化学会考高频考点”的全部内容。本文来源于网络,仅供参考阅读。
相关思维导图模板


树图思维导图提供 904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查 在线思维导图免费制作,点击“编辑”按钮,可对 904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:10b9a8a2dd2fb4593f8130ef16c320fc

树图思维导图提供 9.战斗的基督教 在线思维导图免费制作,点击“编辑”按钮,可对 9.战斗的基督教 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:33d168acd0cd9f767f809c7a5df86e3a









 上海工商
上海工商