蛋白质化学思维导图
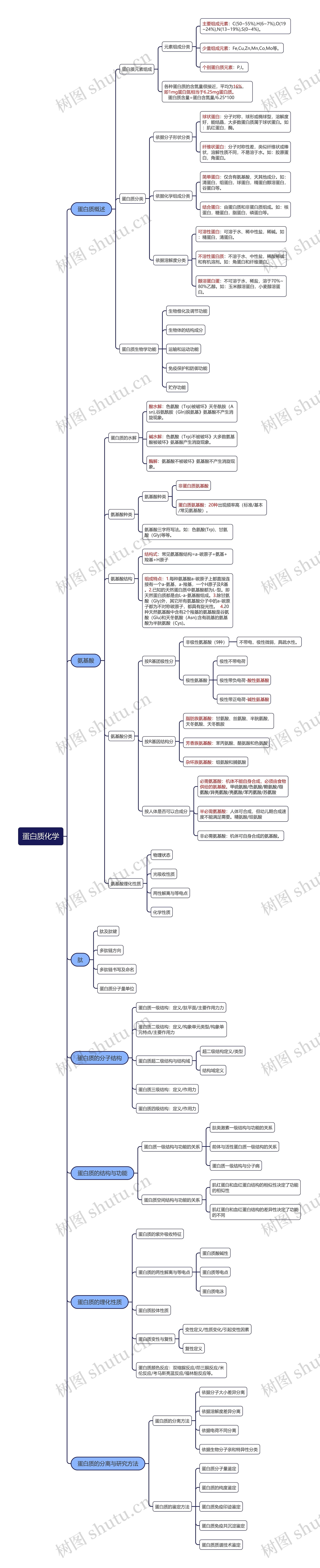
蛋白质化学
树图思维导图提供 蛋白质化学 在线思维导图免费制作,点击“编辑”按钮,可对 蛋白质化学 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:0bb725663209003c5af7f57a6e37d813
思维导图大纲
蛋白质化学思维导图模板大纲
蛋白质概述
蛋白质元素组成
元素组成分类
主要组成元素:C(50~55%),H(6~7%),O(19~24%),N(13~19%),S(0~4%)。
少量组成元素:Fe,Cu,Zn,Mn,Co,Mo等。
个别蛋白质元素:P,I。
各种蛋白质的含氮量很接近,平均为16%,即1mg蛋白氮相当于6.25mg蛋白质。 蛋白质含量=蛋白含氮量/6.25*100
蛋白质分类
依据分子形状分类
球状蛋白:分子对称,球形或椭球型,溶解度好,能结晶,大多数蛋白质属于球状蛋白。如:肌红蛋白,酶。
纤维状蛋白:分子对称性差,类似纤维状或棒状,溶解性质不同,不易溶于水。如:胶原蛋白,角蛋白。
依据化学组成分类
简单蛋白:仅含有氨基酸,天其他成分。如:清蛋白,组蛋白,球蛋白,精蛋白醇溶蛋白,谷蛋白等。
结合蛋白:由蛋白质和非蛋白质组成。如:核蛋白,糖蛋白,脂蛋白,磷蛋白等。
依据溶解度分类
可溶性蛋白:可溶于水、稀中性盐,稀碱。如:精蛋白,清蛋白。
不溶性蛋白质:不溶于水、中性盐,稀酸稀碱和有机溶剂。如:角蛋白和纤维蛋白。
醇溶蛋白蛋:不可溶于水,稀盐,溶于70%~80%乙醇。如:玉米醇溶蛋白,小麦醇溶蛋白。
蛋白质生物学功能
生物倠化及调节功能
生物体的结构成分
运输和运动功能
免疫保护和防御功能
贮存功能
氨基酸
蛋白质的水解
酸水解:色氨酸(Trp)被破坏》天冬酰胺(Asn),谷氨酰胺(Gln)脱氨基》氨基酸不产生消旋现象。
碱水解:色氨酸(Trp)不被破坏》大多数氨基酸被破坏》氨基酸产生消旋现象。
酶解:氨基酸不被破坏》氨基酸不产生消旋现象。
氨基酸种类
氨基酸种类
非蛋白质氨基酸
蛋白质氨基酸:20种出现频率高(标准/基本/常见氨基酸)。
氨基酸三字符写法。如:色氨酸(Trp)、甘氨酸(Gly)等等。
氨基酸结构
结构式:常见氨基酸结构=a-碳原子+氨基+羧基+H原子
组成特点:1.每种氨基酸a-碳原子上都直接连接有一个a-氨基,a-羧基,一个H原子及R基。2.已知的天然蛋白质中氨基酸都为L-型。即天然蛋白质都是由L-a-氨基酸组成。3.除甘氨酸(Gly)外,其它所有氨基酸分子中的a-碳原子都为不对称碳原子,都具有旋光性。 4.20种天然氨基酸中含有2个羧基的氨基酸是谷氨酸(Glu)和天冬氨酸(Asn);含有疏基的氨基酸为半胱氨酸(Cys)。
氨基酸分类
按R基团极性分
非极性氨基酸(9种)
不带电,极性微弱,具疏水性。
极性氨基酸
极性不带电荷
极性带负电荷-酸性氨基酸
极性带正电荷-碱性氨基酸
按R基因结构分
脂肪族氨基酸:甘氨酸、丝氨酸、半胱氨酸、天冬氨酸、天冬酰胺
芳香族氨基酸:苯丙氨酸、酪氨酸和色氨酸
杂环族氨基酸:组氨酸和脯氨酸
按人体是否可以合成分
必需氨基酸:机体不能自身合成,必须由食物供给的氨基酸。甲硫氨酸/色氨酸/赖氨酸/缬氨酸/异亮氨酸/亮氨酸/苯丙氨酸/苏氨酸
半必需氨基酸:人体可合成,但幼儿期合成速度不能满足需要。精氨酸/组氨酸
非必需氨基酸:机体可自身合成的氨基酸。
氨基酸理化性质
物理状态
光吸收性质
两性解离与等电点
化学性质
肽
肽及肽键
多肽链方向
多肽链书写及命名
蛋白质分子量单位
蛋白质的分子结构
蛋白质一级结构:定义/肽平面/主要作用力力
蛋白质二级结构:定义/构象单元类型/构象单元特点/主要作用力
蛋白质超二级结构与结构域
超二级结构定义/类型
结构域定义
蛋白质三级结构:定义/作用力
蛋白质四级结构:定义/作用力
蛋白质的结构与功能
蛋白质一级结构与功能的关系
肽类激素一级结构与功能的关系
前体与活性蛋白质一级结构的关系
蛋白质一级结构与分子病
蛋白质空间结构与功能的关系
肌红蛋白和血红蛋白结构的相似性决定了功能的相似性
肌红蛋白和血红蛋白结构的差异性决定了功能的不同
蛋白质的理化性质
蛋白质的紫外吸收特征
蛋白质的两性解离与等电点
蛋白质酸碱性
蛋白质等电点
蛋白质电泳
蛋白质胶体性质
蛋白质变性与复性
变性定义/性质变化/引起变性因素
复性定义
蛋白质颜色反应:双缩脲反应/茚三酮反应/米伦反应/考马斯亮蓝反应/福林酚反应等。
蛋白质的分离与研究方法
蛋白质的分离方法
依据分子大小差异分离
依据溶解度差异分离
依据电荷不同分离
依据生物分子亲和特异性分类
蛋白质的鉴定方法
蛋白质分子量鉴定
蛋白质的纯度鉴定
蛋白质免疫印迹鉴定
蛋白质免疫共沉淀鉴定
蛋白质质谱技术鉴定
相关思维导图模板


树图思维导图提供 卫生化学--元素和无机物分析 在线思维导图免费制作,点击“编辑”按钮,可对 卫生化学--元素和无机物分析 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:4c942d0350c858e06a1f7ed29a86d096


树图思维导图提供 生化第二章 在线思维导图免费制作,点击“编辑”按钮,可对 生化第二章 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:90ed30dd97ddf19328c0bb40a61b6e11








 上海工商
上海工商