高中化学必修一硅及其化合物 Si思维导图
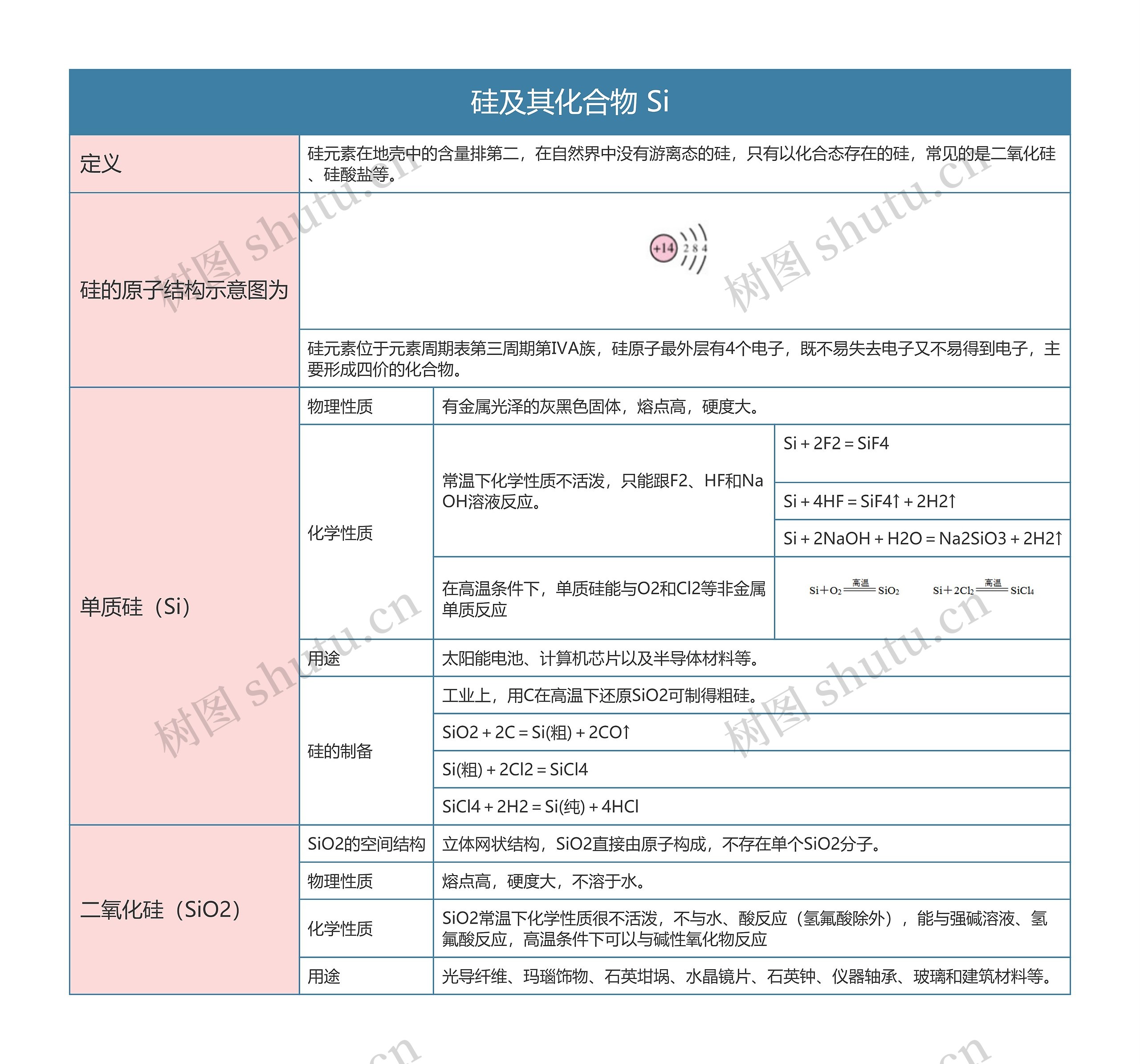
本章节讲述了硅及其化合物 Si的知识点,主要内容包括单质硅(Si)和二氧化硅(SiO2)等
树图思维导图提供 高中化学必修一硅及其化合物 Si思维导图 在线思维导图免费制作,点击“编辑”按钮,可对 高中化学必修一硅及其化合物 Si思维导图 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:4617c2e9bcda11208dd3734ee58d26f1
思维导图大纲
硅及其化合物 Si思维导图模板大纲
定义
硅元素在地壳中的含量排第二,在自然界中没有游离态的硅,只有以化合态存在的硅,常见的是二氧化硅、硅酸盐等。
硅的原子结构示意图为
硅元素位于元素周期表第三周期第ⅣA族,硅原子最外层有4个电子,既不易失去电子又不易得到电子,主要形成四价的化合物。
单质硅(Si)
物理性质
有金属光泽的灰黑色固体,熔点高,硬度大。
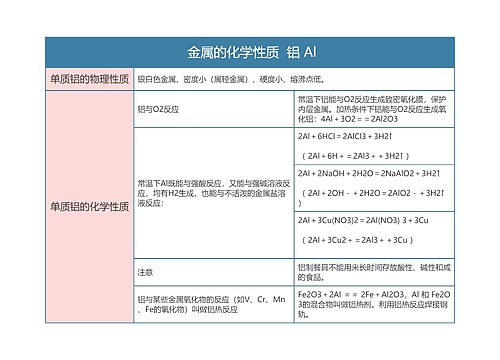
化学性质
常温下化学性质不活泼,只能跟F2、HF和NaOH溶液反应。
Si+2F2=SiF4
Si+4HF=SiF4↑+2H2↑
Si+2NaOH+H2O=Na2SiO3+2H2↑
在高温条件下,单质硅能与O2和Cl2等非金属单质反应
用途
太阳能电池、计算机芯片以及半导体材料等。
硅的制备
工业上,用C在高温下还原SiO2可制得粗硅。
SiO2+2C=Si(粗)+2CO↑
Si(粗)+2Cl2=SiCl4
SiCl4+2H2=Si(纯)+4HCl
二氧化硅(SiO2)
SiO2的空间结构
立体网状结构,SiO2直接由原子构成,不存在单个SiO2分子。
物理性质
熔点高,硬度大,不溶于水。
化学性质
SiO2常温下化学性质很不活泼,不与水、酸反应(氢氟酸除外),能与强碱溶液、氢氟酸反应,高温条件下可以与碱性氧化物反应
用途
光导纤维、玛瑙饰物、石英坩埚、水晶镜片、石英钟、仪器轴承、玻璃和建筑材料等。
相关思维导图模板
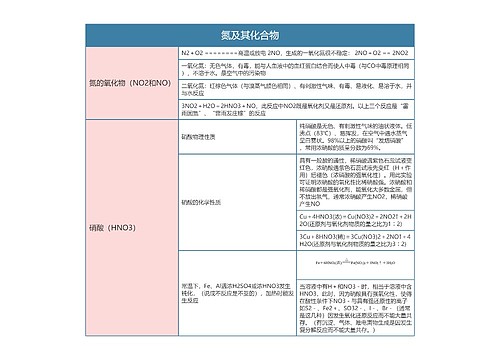

树图思维导图提供 高中化学必修一氮及其化合物思维导图 在线思维导图免费制作,点击“编辑”按钮,可对 高中化学必修一氮及其化合物思维导图 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:a1f5ccff69599a916a48d0ad5d6f2faf


树图思维导图提供 高中化学必修一硫酸(H2SO4)思维导图 在线思维导图免费制作,点击“编辑”按钮,可对 高中化学必修一硫酸(H2SO4)思维导图 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:3ea2e8ba24f45b701c4f48ca23e032a2





 上海工商
上海工商