生物化学思维脑图思维导图
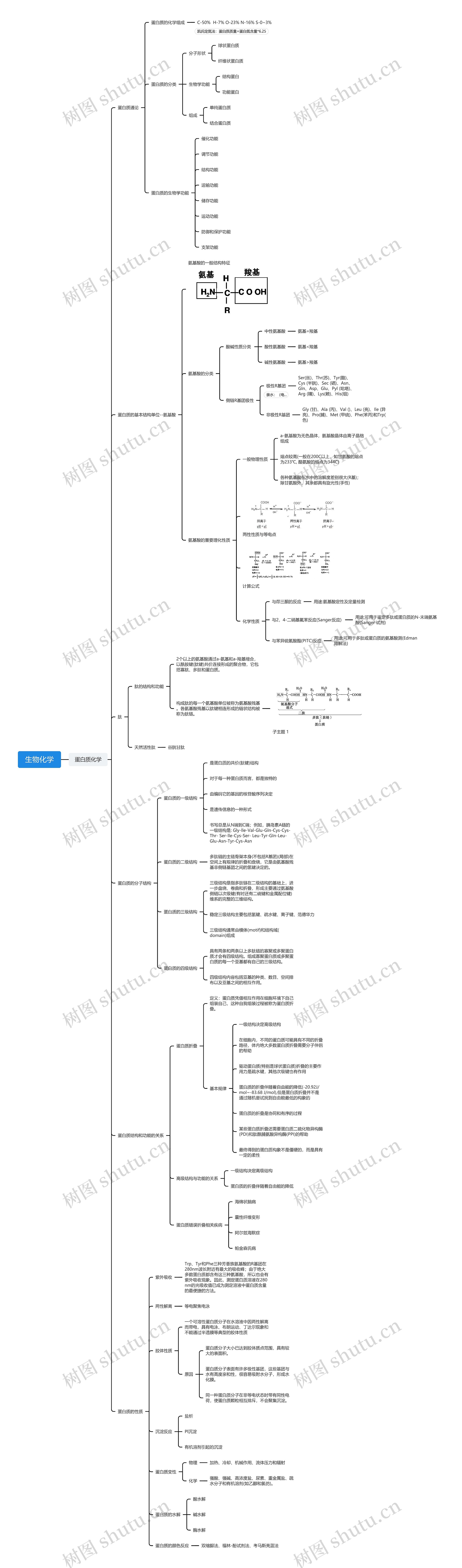
蛋白质通论,结构单位,分子结构等内容讲解
树图思维导图提供 生物化学思维脑图 在线思维导图免费制作,点击“编辑”按钮,可对 生物化学思维脑图 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:59428a50fca4c2a7c924901c27d2827a
思维导图大纲
生物化学思维导图模板大纲
蛋白质化学
蛋白质通论
蛋白质的化学组成
C-50% H-7% O-23% N-16% S-0~3%
蛋白质的分类
分子形状
球状蛋白质
纤维状蛋白质
生物学功能
结构蛋白
功能蛋白
组成
单纯蛋白质
结合蛋白质
蛋白质的生物学功能
催化功能
调节功能
结构功能
运输功能
储存功能
运动功能
防御和保护功能
支架功能
蛋白质的基本结构单位--氨基酸
氨基酸的一般结构特征
氨基酸的分类
酸碱性质分类
中性氨基酸
氨基=羧基
酸性氨基酸
氨基<羧基
碱性氨基酸
氨基>羧基
侧链R基团极性
极性R基团
Ser(丝)、Thr(苏)、Tyr(酪)、Cys (半胱)、Sec (硒)、Asn、Gln、Asp、Glu、Pyl (吡咯)、Arg (精)、Lys(赖)、His(组)
非极性R基团
Gly (甘)、Ala (丙)、Val ()、Leu (亮)、Ile (异亮)、Pro(脯)、Met (甲硫)、Phe(苯丙)和Trp(色)
氨基酸的重要理化性质
一般物理性质
a-氨基酸为无色晶体,氨基酸晶体由离子晶格组成
熔点较高(一般在200C以上,如甘氨酸的熔点为233℃, 酪氨酸的熔点为344C)
各种氨基酸在水中的溶解度差别很大(R基); 除甘氨酸外,其余都具有旋光性(手性)
两性性质与等电点
计算公式
化学性质
与茚三酮的反应
用途:氨基酸定性及定量检测
与2,4-二硝基氟苯反应(Sanger反应)
用途:可用于鉴定多肽或蛋白质的N-末端氨基酸(Sanger 试剂)
与苯异硫氰酸酯(PITC)反应
用途:可用于多肽或蛋白质的氨基酸测(Edman降解法)
肽
肽的结构和功能
2个以上的氨基酸通过a-氨基和a-羧基缩合,以酰胺键(肽键)共价连接形成的聚合物,它包括寡肽、多肽和蛋白质。
构成肽的每一个氨基酸单位被称为氨基酸残基。各氨基酸残基以肽键相连形成的链状结构被称为肽链。
子主题 1
天然活性肽
谷胱甘肽
蛋白质的分子结构
蛋白质的一级结构
是蛋白质的共价(肽键)结构
对于每一种蛋白质而言,都是独特的
由编码它的基因的核苷酸序列决定
是遗传信息的一种形式
书写总是从N端到C端;例如,胰岛素A链的一级结构是: Gly-lle-Val-Glu-Gln-Cys-Cys-Thr- Ser-lle-Cys-Ser- Leu-Tyr-GIn-Leu-Glu-Asn-Tyr-Cys-Asn
蛋白质的二级结构
多肽链的主链骨架本身(不包括R基团)(局部)在空间上有规律的折叠和盘绕,它是由氨基酸残基非侧链基团之间的氢键决定的。
蛋白质的三级结构
三级结构是指多肽链在二级结构的基础上,进一步盘绕、卷曲和折叠,形成主要通过氨基酸侧链以次级键(有时还有二硫键和金属配位键)维系的完整的三维结构。
稳定三级结构主要包括氢键、疏水键、离子键、范德华力
三级结构通常由模体(motif)和结构域(domain)组成
蛋白质的四级结构
具有两条和两条以上多肽链的寡聚或多聚蛋白质才会有四级结构。组成寡聚蛋白质或多聚蛋白质的每一个亚基都有自己的三级结构。
四级结构内容包括亚基的种类、数目、空间排布以及亚基之间的相互作用。
蛋白质结构和功能的关系
蛋白质折叠
定义:蛋白质凭借相互作用在细胞环境下自己组装自己,这种自我组装过程被称为蛋白质折叠。
基本规律
一级结构决定高级结构
在细胞内,不同的蛋白质可能具有不同的折叠路径,体内绝大多数蛋白质折叠需要分子伴侣的帮助
驱动蛋白质(特别是球状蛋白质)折叠的主要作用力是疏水键,其他次级键也有作用
蛋白质的折叠伴随着自由能的降低(-20.92J/mol~-83.68 J/mol),但是蛋白质折叠并不是通过随机尝试找到自由能最低的构象的
蛋白质的折叠是协同和有序的过程
某些蛋白质折叠还需要蛋白质二硫化物异构酶(PDI)和肽酰脯氨酸异构酶(PPI)的帮助
最终得到的蛋白质构象不是僵硬的,而是具有一定的柔性
高级结构与功能的关系
一级结构决定高级结构
蛋白质的折叠伴随着自由能的降低
蛋白质错误折叠相关疾病
海绵状脑病
囊性纤维变形
阿尔兹海默症
帕金森氏病
蛋白质的性质
紫外吸收
Trp、Tyr和Phe三种芳香族氨基酸的R基团在280nm波长附近有最大的吸收峰;由于绝大多数蛋白质都含有这三种氨基酸,所以也会有紫外吸收现象。因此,测定蛋白质溶液在280nm的光吸收值已成为测定溶液中蛋白质含量的最便捷的方法。
两性解离
等电聚焦电泳
胶体性质
一个可溶性蛋白质分子在水溶液中因两性解离而带电,具有电泳、布朗运动、丁达尔现象和不能通过半透膜等典型的胶体性质
原因
蛋白质分子大小已达到胶体质点范围,具有较大的表面积。
蛋白质分子表面有许多极性基团,这些基团与水有高度亲和性,很容易吸附水分子,形成水化膜。
同一种蛋白质分子在非等电状态时带有同性电荷,使蛋白质颗粒相互排斥,不会聚集沉淀。
沉淀反应
盐析
Pl沉淀
有机溶剂引起的沉淀
蛋白质变性
物理
加热、冷却、机械作用、流体压力和辐射
化学
强酸、强碱、高浓度盐、尿素、重金属盐、疏水分子和有机溶剂(如乙醇和氯仿)。
蛋白质的水解
酸水解
碱水解
酶水解
蛋白质的颜色反应
双缩脲法、福林-酚试剂法、考马斯亮蓝法
相关思维导图模板

树图思维导图提供 1107文家市玉萍思维导图 在线思维导图免费制作,点击“编辑”按钮,可对 1107文家市玉萍思维导图 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:ed943ef641f6dc874860eb6095857ed6

树图思维导图提供 种子思维脑图 在线思维导图免费制作,点击“编辑”按钮,可对 种子思维脑图 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:86f8307a40ea24607c6c79354e09377f







 上海工商
上海工商