“溶液”知识梳理思维导图

介绍“溶液”知识梳理
树图思维导图提供 “溶液”知识梳理 在线思维导图免费制作,点击“编辑”按钮,可对 “溶液”知识梳理 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:c5059f77274cdfb0697b990e722dbd3f
思维导图大纲
“溶液”知识梳理思维导图模板大纲
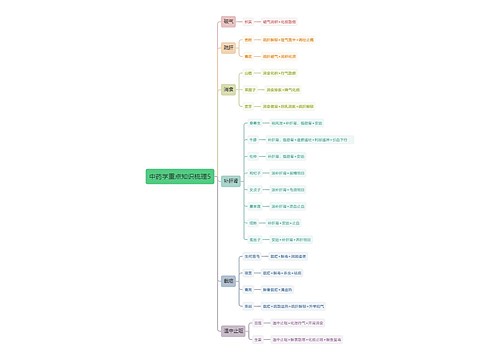
溶液的形成
1、溶液
1.溶液的特点:均一性、稳定性、混合物;
2.溶液由溶质和溶剂组成;m溶液=m溶质+m溶剂
3.注意:
(1)溶液不一定是无色的,比如硫酸铜溶液(蓝色),硫酸亚铁溶液(浅绿色);
(2)水、无水乙醇是纯净物,不属于溶液。
2、溶解时的吸放热现象
1.溶解放热的代表物质:NaOH、浓硫酸(氧化钙与水反应发生化学变化而放热、镁与稀盐酸反应放热)。
2.溶解时吸热的代表物质NH4NO3;
3.溶解时无明显吸、放热现象物质 NaCl;
注意:做题时要考虑吸放热对密闭容器内压强变化的影响。
饱和溶液与不饱和溶液
1、判断
在一定温度下,向一定量的溶剂中加入某种溶质,当溶质不在继续溶解时,此时为该溶质的饱和溶液,如果还能继续溶解,则为该溶质的不饱和溶液(实验图考查较多)。
2、转换
1. 适用于大多数固体(溶解度随温度升高而增大的物质)
2. 适用于极少数固体(溶解度随温度升高而减小的物质,比如氢氧化钙)
3、结晶方法
1.蒸发结晶:适用于溶解度受温度影响较小的物质,比如氯化钠;
2.降温结晶(冷却热饱和溶液):适用于溶解度随温度升高而增大,且受温度影响较大的物质,比如硝酸钾。
3.一种物质中含另一种物质,想得到其中一种物质的晶体。
口诀:大中有小,降温结晶;小中有大,蒸发结晶。(“大”指的是溶解度受温度影响较大的物质,“小”指的是受温度影响较小的物质)。
溶解度
1、固体溶解度
1.定义:在一定温度下,某固体物质在100g溶剂里达到饱和状态时所溶解的质量,单位为“g”。
2.影响因素:
(1)内因:溶质、溶剂的性质
(2)外因:温度
2、气体溶解度
1.定义:该气体的压强在101Kpa和一定温度下,在1体积水里溶解达到饱和状态时的气体体积。
2.影响因素:
(1)内因:气体、溶剂的性质
(2)外因:压强(气体溶解度与压强成正比)、温度(气体溶解度与温度成反比)。
溶解度曲线
1.查找某种物质的溶解度,该物质在某一温度下曲线上点对应的纵坐标值。
2.比较不同物质在同一温度下溶解度的大小,同一温度下,位于上方曲线对应物质的溶解度大于下方曲线对应物质的溶解度。
注意:比较溶解度,前提是确定温度。
3.判断物质的溶解度随温度变化的曲线
分析溶解度曲线的坡度及走势,从左向右看曲线的走势是向上、向下还是趋于平缓。 常见代表物质:陡升型:硝酸钾。缓升型:氯化钠。下降型:氢氧化钙
相关思维导图模板
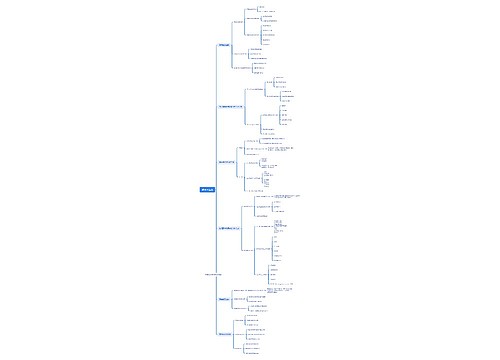

树图思维导图提供 高分子溶液 在线思维导图免费制作,点击“编辑”按钮,可对 高分子溶液 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:10aaee847ae70a6508dd60eccfca448d
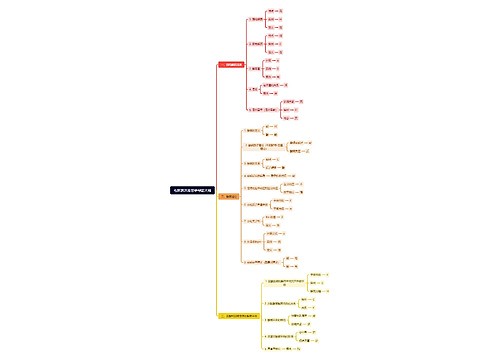

树图思维导图提供 电解质溶液思维导图大纲 在线思维导图免费制作,点击“编辑”按钮,可对 电解质溶液思维导图大纲 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:527447dec8ac7f31bca00f3656d02143











 上海工商
上海工商