药物临床前研究政策思维导图

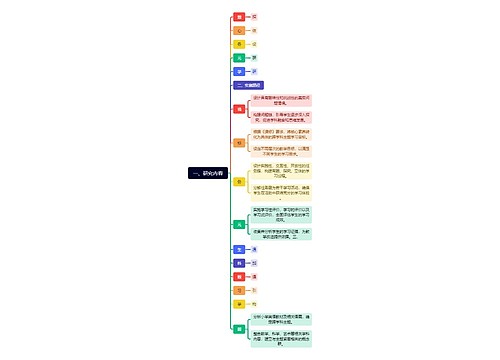
第二十一条 为申请药品注册而进行的药物临床前研究,包括药物的合成工艺、提取方法、理化性质及纯度、剂型选择、处方筛选、制备工艺、检验方法、质量指标、稳定性、药理、毒理、动物药代动力学研究等。
树图思维导图提供 药物临床前研究政策 在线思维导图免费制作,点击“编辑”按钮,可对 药物临床前研究政策 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:a4979fd2547bcd855fbc9746bbfcbc64
思维导图大纲
药物临床前研究政策思维导图模板大纲
第二十一条 为申请药品注册而进行的药物临床前研究,包括药物的合成工艺、提取方法、理化性质及纯度、剂型选择、处方筛选、制备工艺、检验方法、质量指标、稳定性、药理、毒理、动物药代动力学研究等。中药制剂还包括原药材的来源、加工及炮制等的研究;生物制品还包括菌毒种、细胞株、生物组织等起始原材料的来源、质量标准、保存条件、生物学特征、遗传稳定性及免疫学的研究等。
第二十二条 药物临床前研究应当执行有关管理规定,医学教|育网搜集整理其中安全性评价研究必须执行《药物非临床研究质量管理规范》。
第二十三条 药物研究机构应当具有与试验研究项目相适应的人员、场地、设备、仪器和管理制度,并保证所有试验数据和资料的真实性;所用实验动物、试剂和原材料应当符合国家有关规定和要求。
第二十四条 申请人委托其他机构进行药物研究或者进行单项试验、检测、样品的试制等的,应当与被委托方签订合同,并在申请注册时予以说明。申请人对申报资料中的药物研究数据的真实性负责。
第二十五条 单独申请注册药物制剂的,研究用原料药必须具有药品批准文号、《进口药品注册证》或者《医药产品注册证》,且必须通过合法的途径获得。研究用原料药不具有药品批准文号、《进口药品注册证》或者《医药产品注册证》的,必须经国家食品药品监督管理局批准。








 上海工商
上海工商