《法规》重要考点:医疗器械不良事件的处理与问题产品的召回思维导图

树图网
树图思维导图提供 《法规》重要考点:医疗器械不良事件的处理与问题产品的召回 在线思维导图免费制作,点击“编辑”按钮,可对 《法规》重要考点:医疗器械不良事件的处理与问题产品的召回 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:1181ae769692680cf4d22f366c9b5acb
思维导图大纲
《法规》重要考点:医疗器械不良事件的处理与问题产品的召回思维导图模板大纲
为了帮助大家备考,树图网为大家整理出如下相关内容:
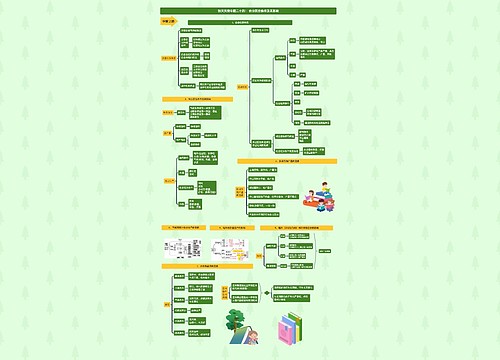
医疗器械不良事件监测和再评价
(1)报告原则:可疑即报。
(2)个例医疗器械不良事件报告时限要求
①注册人、备案人、生产经营企业、使用单位发现或获知导致死亡的可疑不良事件的,应在7日内报告;导致严重伤害、可能导致严重伤害或死亡的,应在20日内报告。②境外持有人和在境外销售国产医疗器械的持有人发现或获知在境外发生的导致或可能导致严重伤害或者死亡的可疑不良事件的,应在30日内报告。
(3)群体医疗器械不良事件报告的时限要求
注册人、备案人、生产经营企业、使用单位发现或获知群体不良事件后,应在12小时内报告不良事件发生地省(区、市)药品监管部门和卫生健康主管部门,必要时可越级报告。
通过国家医疗器械不良事件监测信息网络报告群体不良事件基本信息,对每一事件还应在24小时内按个例事件报告。
持有人应当立即暂停生产、销售,开展自查,通知使用单位停止使用相关产品,自查结果于7日内向所在地及不良事件发生地省(区、市)药品监管部门和监测机构报告。经营企业、使用单位应当在12小时内告知持有人,启动自查并配合持有人调查。
相关思维导图模板


树图思维导图提供 904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查 在线思维导图免费制作,点击“编辑”按钮,可对 904名中国成年人第三磨牙相关知识、态度、行为和病史的横断面调查 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:10b9a8a2dd2fb4593f8130ef16c320fc

树图思维导图提供 9.战斗的基督教 在线思维导图免费制作,点击“编辑”按钮,可对 9.战斗的基督教 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:33d168acd0cd9f767f809c7a5df86e3a







 上海工商
上海工商