高一化学必修二知识点归纳总结思维导图
高中阶段学习难度、强度、容量加大,学习负担及压力明显加重,不能再依赖初中时期老师“填鸭式”的授课,“看管式”的自习,“命令式”的作业,要逐步培养自己主动获取知识、巩固知识的能力,制定学习计划,养成自主学习的好习惯。今天树图网高一频道为正在拼搏的你整理了《高一化学必修二知识点归纳总结》,希望以下内容可以帮助到您!
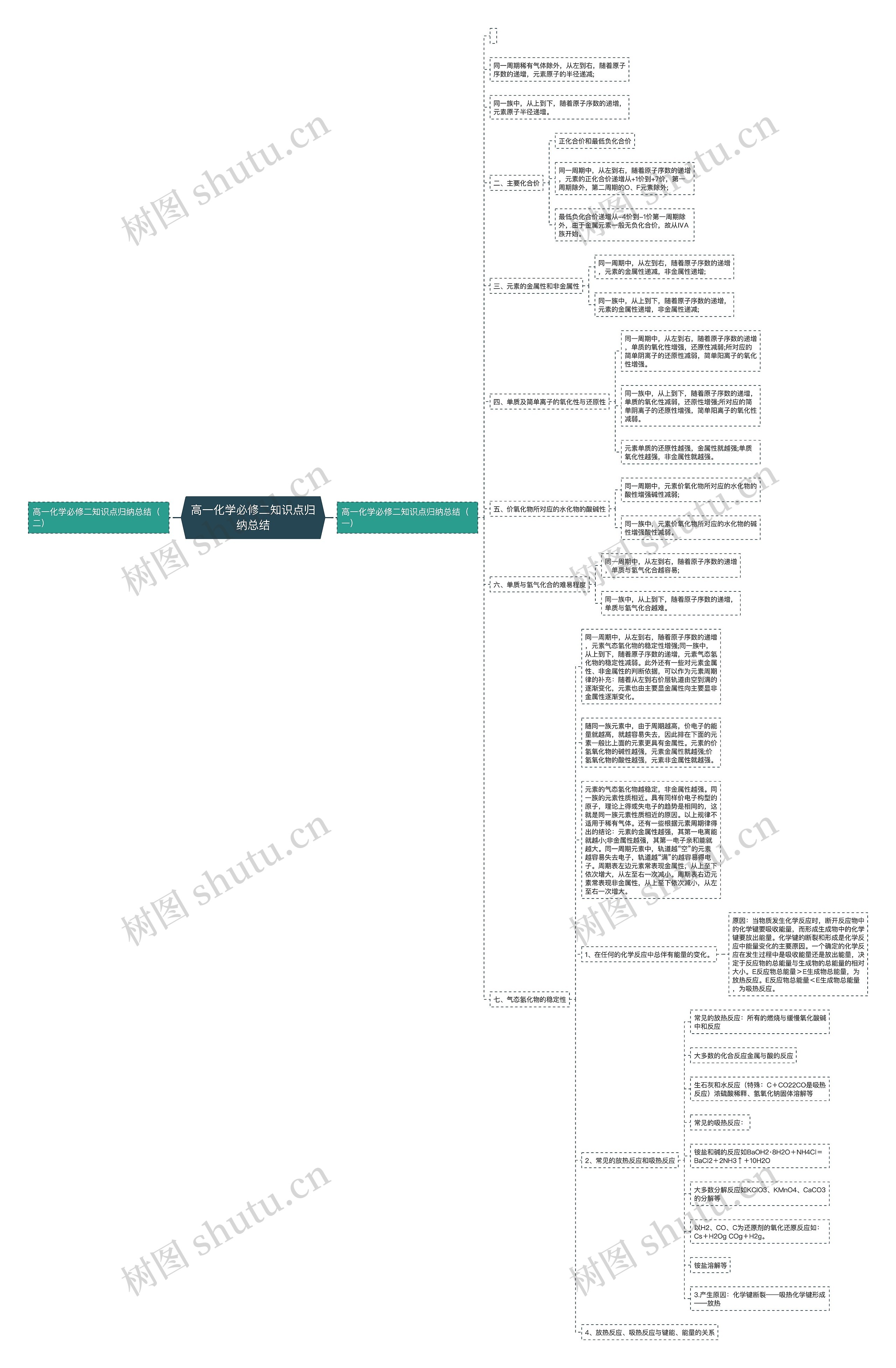
树图思维导图提供 高一化学必修二知识点归纳总结 在线思维导图免费制作,点击“编辑”按钮,可对 高一化学必修二知识点归纳总结 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:6ea54c07092e1692ebb9b59fdda037ac
思维导图大纲
高一化学必修二知识点归纳总结思维导图模板大纲
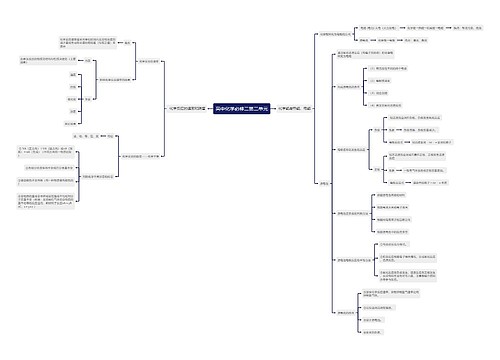
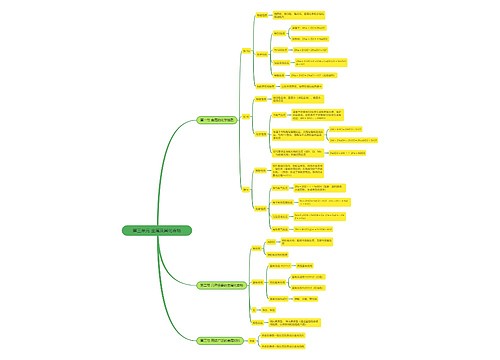
高一化学必修二知识点归纳总结(一)
同一周期稀有气体除外,从左到右,随着原子序数的递增,元素原子的半径递减;
同一族中,从上到下,随着原子序数的递增,元素原子半径递增。
二、主要化合价
正化合价和最低负化合价
同一周期中,从左到右,随着原子序数的递增,元素的正化合价递增从+1价到+7价,第一周期除外,第二周期的O、F元素除外;
最低负化合价递增从-4价到-1价第一周期除外,由于金属元素一般无负化合价,故从ⅣA族开始。
三、元素的金属性和非金属性
同一周期中,从左到右,随着原子序数的递增,元素的金属性递减,非金属性递增;
同一族中,从上到下,随着原子序数的递增,元素的金属性递增,非金属性递减;
四、单质及简单离子的氧化性与还原性
同一周期中,从左到右,随着原子序数的递增,单质的氧化性增强,还原性减弱;所对应的简单阴离子的还原性减弱,简单阳离子的氧化性增强。
同一族中,从上到下,随着原子序数的递增,单质的氧化性减弱,还原性增强;所对应的简单阴离子的还原性增强,简单阳离子的氧化性减弱。
元素单质的还原性越强,金属性就越强;单质氧化性越强,非金属性就越强。
五、价氧化物所对应的水化物的酸碱性
同一周期中,元素价氧化物所对应的水化物的酸性增强碱性减弱;
同一族中,元素价氧化物所对应的水化物的碱性增强酸性减弱。
六、单质与氢气化合的难易程度
同一周期中,从左到右,随着原子序数的递增,单质与氢气化合越容易;
同一族中,从上到下,随着原子序数的递增,单质与氢气化合越难。
七、气态氢化物的稳定性
同一周期中,从左到右,随着原子序数的递增,元素气态氢化物的稳定性增强;同一族中,从上到下,随着原子序数的递增,元素气态氢化物的稳定性减弱。此外还有一些对元素金属性、非金属性的判断依据,可以作为元素周期律的补充:随着从左到右价层轨道由空到满的逐渐变化,元素也由主要显金属性向主要显非金属性逐渐变化。
随同一族元素中,由于周期越高,价电子的能量就越高,就越容易失去,因此排在下面的元素一般比上面的元素更具有金属性。元素的价氢氧化物的碱性越强,元素金属性就越强;价氢氧化物的酸性越强,元素非金属性就越强。
元素的气态氢化物越稳定,非金属性越强。同一族的元素性质相近。具有同样价电子构型的原子,理论上得或失电子的趋势是相同的,这就是同一族元素性质相近的原因。以上规律不适用于稀有气体。还有一些根据元素周期律得出的结论:元素的金属性越强,其第一电离能就越小;非金属性越强,其第一电子亲和能就越大。同一周期元素中,轨道越“空”的元素越容易失去电子,轨道越“满”的越容易得电子。周期表左边元素常表现金属性,从上至下依次增大,从左至右一次减小。周期表右边元素常表现非金属性,从上至下依次减小,从左至右一次增大。
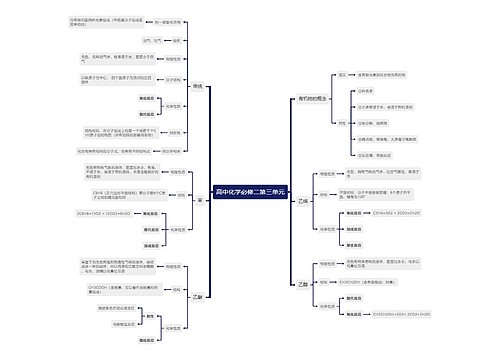
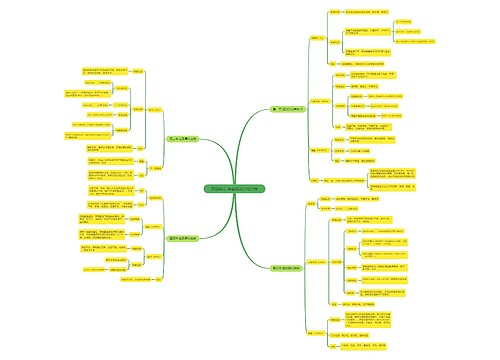
1、在任何的化学反应中总伴有能量的变化。
原因:当物质发生化学反应时,断开反应物中的化学键要吸收能量,而形成生成物中的化学键要放出能量。化学键的断裂和形成是化学反应中能量变化的主要原因。一个确定的化学反应在发生过程中是吸收能量还是放出能量,决定于反应物的总能量与生成物的总能量的相对大小。E反应物总能量>E生成物总能量,为放热反应。E反应物总能量<E生成物总能量,为吸热反应。
2、常见的放热反应和吸热反应
常见的放热反应:所有的燃烧与缓慢氧化酸碱中和反应
大多数的化合反应金属与酸的反应
生石灰和水反应(特殊:C+CO22CO是吸热反应)浓硫酸稀释、氢氧化钠固体溶解等
常见的吸热反应:
铵盐和碱的反应如BaOH2·8H2O+NH4Cl=BaCl2+2NH3↑+10H2O
大多数分解反应如KClO3、KMnO4、CaCO3的分解等
以H2、CO、C为还原剂的氧化还原反应如:Cs+H2Og COg+H2g。
铵盐溶解等
3.产生原因:化学键断裂——吸热化学键形成——放热
4、放热反应、吸热反应与键能、能量的关系
高一化学必修二知识点归纳总结(二)
相关思维导图模板

树图思维导图提供 1113爆卡会总结会会议纪要 在线思维导图免费制作,点击“编辑”按钮,可对 1113爆卡会总结会会议纪要 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:aaf6c152a765d5821e8e1787f2b3226e

树图思维导图提供 人教版必修一:分子与细胞 在线思维导图免费制作,点击“编辑”按钮,可对 人教版必修一:分子与细胞 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:38b99f99a660f9eb846aafd51549cc03





 上海工商
上海工商