化学选修三微粒半径思维导图

部编版高中化学选修三中有关微粒半径的思维导图,包括非金属性强弱的判断方法等
树图思维导图提供 化学选修三微粒半径思维导图 在线思维导图免费制作,点击“编辑”按钮,可对 化学选修三微粒半径思维导图 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:66d31c21b30f2fb5a449493f8d67cc1e
思维导图大纲
化学选修三微粒半径思维导图思维导图模板大纲
同一元素
一般情况下元素阴离子的离子半径大于相应原子的原子半径,阳离子的离子半径小于相应原子的原子半径
同周期元素(只能比较原子半径)
随原子序数的增大,原子的原子半径依次减小
如:Na>Mg>Al>Si>P>S>C
同主族元素(比较原子和离子半径)
随原子序数的增大,原子的原子半径依次增大
如:Li<Na<K<Rb<Cs,F-<Cl-<Br-<I-
同电子层结构
随核电荷数增大,微粒半径依 次减小
如:F-> Na+>Mg2+>Al3+
元素金属性强弱的判断方法
本质
原子越易失电子,金属性越强
判断依据
在金属活动顺序表中越靠前,金属性越强
单质与水或非氧化性酸反应越剧烈,金属性越强
单质还原性越强或离子氧化性越弱,金属性越强
电解中在阴极上得电 子的先后
最高价氧化物对应水化物的碱性越强,金属性越强
原电池反应中负极的金属性强
与同种氧化剂反应,先反应的金属性强
失去相同数目的电子,吸收能量少的金属性强
非金属性强弱的判断方法
本质
原子越易得电子,非金属性越强
判断方法
与 H2 化合越易,气态氢化物越稳定,非金属性越强
单质氧化性越强,阴离子还原性越弱,非金属性越强
电解中在阳极 上得电子的先后
最高价氧化物的水化物酸性越强,非金属性越强
与同种还原剂反应,先反应的非金属性强
相关思维导图模板
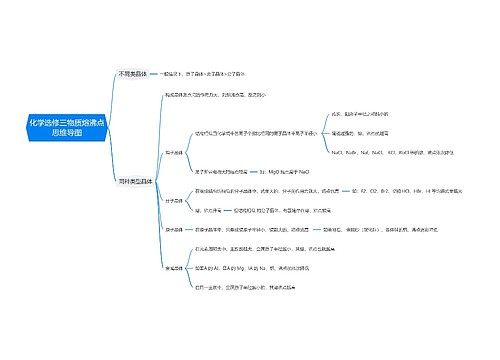
树图思维导图提供 化学选修三物质熔沸点思维导图 在线思维导图免费制作,点击“编辑”按钮,可对 化学选修三物质熔沸点思维导图 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:284b57a4453deced2e7136e60e3ded85

树图思维导图提供 化学选修三典型晶体思维导图 在线思维导图免费制作,点击“编辑”按钮,可对 化学选修三典型晶体思维导图 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:5e8e57e9e2839cb9b45797c670b8c719





 上海工商
上海工商