配位化合物及配位平衡思维导图
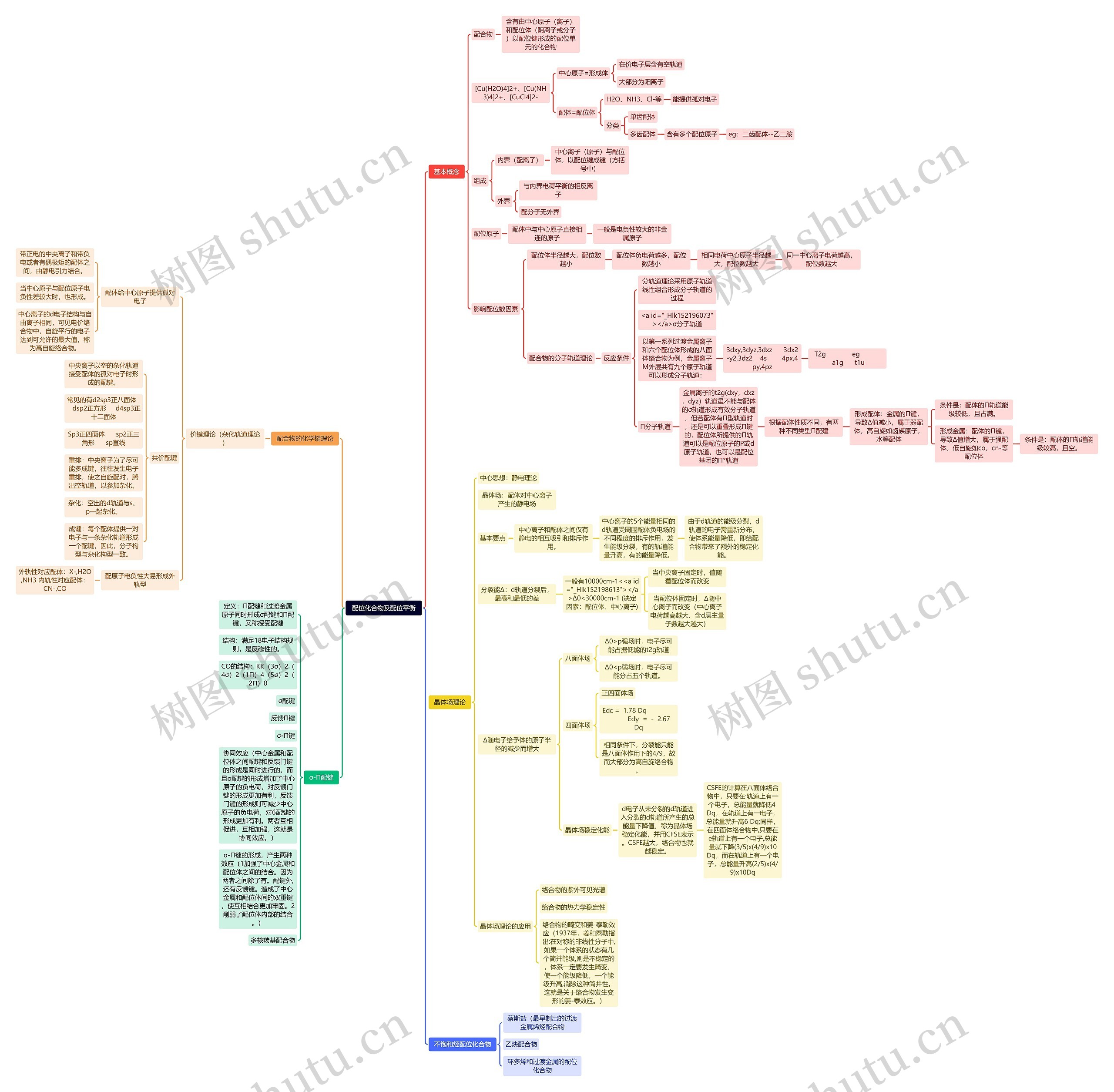
配合物化学键理论,晶体场理论等内容分解
树图思维导图提供 配位化合物及配位平衡 在线思维导图免费制作,点击“编辑”按钮,可对 配位化合物及配位平衡 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:fc4acb17edd78e123e26f5f0c6bbb86e
思维导图大纲
配位化合物及配位平衡思维导图模板大纲
基本概念
配合物
含有由中心原子(离子)和配位体(阴离子或分子)以配位键形成的配位单元的化合物
[Cu(H2O)4]2+、[Cu(NH3)4]2+、[CuCl4]2-
中心原子=形成体
在价电子层含有空轨道
大部分为阳离子
配体=配位体
H2O、NH3、Cl-等
能提供孤对电子
分类
单齿配体
多齿配体
含有多个配位原子
eg:二齿配体--乙二胺
组成
内界(配离子)
中心离子(原子)与配位体,以配位键成键(方括号中)
外界
与内界电荷平衡的相反离子
配分子无外界
配位原子
配体中与中心原子直接相连的原子
一般是电负性较大的非金属原子
影响配位数因素
配位体半径越大,配位数越小
配位体负电荷越多,配位数越小
相同电荷中心原子半径越大,配位数越大
同一中心离子电荷越高,配位数越大
配合物的分子轨道理论
反应条件
分轨道理论采用原子轨道线性组合形成分子轨道的过程
<a id="_Hlk152196073"></a>σ分子轨道
以第一系列过渡金属离子和六个配位体形成的八面体络合物为例,金属离子M外层共有九个原子轨道可以形成分子轨道:
3dxy,3dyz,3dxz 3dx2-y2,3dz2 4s 4px,4py,4pz
T2g eg a1g t1u
Π分子轨道
金属离子的t2g(dxy,dxz,dyz)轨道虽不能与配体的σ轨道形成有效分子轨道,但若配体有Π型轨道时,还是可以重叠形成Π键的,配位体所提供的Π轨道可以是配位原子的P或d原子轨道,也可以是配位基团的Π*轨道
根据配体性质不同,有两种不同类型Π配建
形成配体:金属的Π键,导致Δ值减小,属于弱配体,高自旋如卤族原子,水等配体
条件是:配体的Π轨道能级较低,且占满。
形成金属:配体的Π键,导致Δ值增大,属于强配体,低自旋如co,cn-等配位体
条件是:配体的Π轨道能级较高,且空。
配合物的化学键理论
价键理论(杂化轨道理论)
配体给中心原子提供孤对电子
带正电的中央离子和带负电或者有偶极矩的配体之间,由静电引力结合。
当中心原子与配位原子电负性差较大时,也形成。
中心离子的d电子结构与自由离子相同,可见电价络合物中,自旋平行的电子达到可允许的最大值,称为高自旋络合物。
共价配键
中央离子以空的杂化轨道接受配体的孤对电子时形成的配键。
常见的有d2sp3正八面体 dsp2正方形 d4sp3正十二面体
Sp3正四面体 sp2正三角形 sp直线
重排:中央离子为了尽可能多成键,往往发生电子重排,使之自旋配对,腾出空轨道,以参加杂化。
杂化:空出的d轨道与s、p一起杂化。
成键:每个配体提供一对电子与一条杂化轨道形成一个配键,因此,分子构型与杂化构型一致。
配原子电负性大易形成外轨型
外轨性对应配体:X-,H2O,NH3 内轨性对应配体:CN-,CO
晶体场理论
中心思想:静电理论
晶体场:配体对中心离子产生的静电场
基本要点
中心离子和配体之间仅有静电的相互吸引和排斥作用。
中心离子的5个能量相同的d轨道受周围配体负电场的不同程度的排斥作用,发生能级分裂,有的轨道能量升高,有的能量降低。
由于d轨道的能级分裂,d轨道的电子需重新分布,使体系能量降低,即给配合物带来了额外的稳定化能。
分裂能Δ:d轨道分裂后,最高和最低的差
一般有10000cm-1<<a id="_Hlk152198613"></a>Δ0<30000cm-1 (决定因素:配位体、中心离子)
当中央离子固定时,值随着配位体而改变
当配位体固定时,Δ随中心离子而改变(中心离子电荷越高越大、含d层主量子数越大越大)
Δ随电子给予体的原子半径的减少而增大
八面体场
Δ0>p强场时,电子尽可能占据低能的t2g轨道
Δ0<p弱场时,电子尽可能分占五个轨道。
四面体场
正四面体场
Edε = 1.78 Dq Edγ = - 2.67 Dq
相同条件下,分裂能只能是八面体作用下的4/9,故而大部分为高自旋络合物。
晶体场稳定化能
d电子从未分裂的d轨道进入分裂的d轨道所产生的总能量下降值,称为晶体场稳定化能,并用CFSE表示。CSFE越大,络合物也就越稳定。
CSFE的计算在八面体络合物中,只要在:轨道上有一个电子,总能量就降低4 Dq,在轨道上有一电子,总能量就升高6 Dq;同样,在四面体络合物中,只要在e轨道上有一个电子,总能量就下降(3/5)x(4/9)x10Dq,而在轨道上有一个电子,总能量升高(2/5)x(4/9)x10Dq
晶体场理论的应用
络合物的紫外可见光谱
络合物的热力学稳定性
络合物的畸变和姜-泰勒效应(1937年,姜和泰勒指出:在对称的非线性分子中,如果一个体系的状态有几个简并能级,则是不稳定的,体系一定要发生畸变,使一个能级降低,一个能级升高,消除这种简并性。这就是关于络合物发生变形的姜-泰效应。)
σ-Π配键
定义:Π配键和过渡金属原子同时形成σ配键和Π配键,又称授受配键
结构:满足18电子结构规则,是反磁性的。
CO的结构:KK(3σ)2(4σ)2(1Π)4(5σ)2(2Π)0
σ配键
反馈Π键
σ-Π键
协同效应(中心金属和配位体之间配键和反馈门键的形成是同时进行的,而且o配键的形成增加了中心原子的负电荷,对反馈门键的形成更加有利,反馈门键的形成则可减少中心原子的负电荷,对6配键的形成更加有利。两者互相促进,互相加强,这就是协同效应。)
σ-Π键的形成,产生两种效应(1加强了中心金属和配位体之间的结合。因为两者之间除了有。配键外,还有反馈键。造成了中心金属和配位体间的双重键,使互相结合更加牢固。2削弱了配位体内部的结合。)
多核羰基配合物
不饱和烃配位化合物
蔡斯盐(最早制出的过渡金属烯烃配合物
乙炔配合物
环多烯和过渡金属的配位化合物
相关思维导图模板

树图思维导图提供 广播电视奖项及评奖标准 在线思维导图免费制作,点击“编辑”按钮,可对 广播电视奖项及评奖标准 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:a4210651fa3a78355ac9f5101bb2c616









 上海工商
上海工商