分析化学 配位滴定法思维导图
免费下载
免费使用文件
。 浏览量:222022-11-16 13:26:25
已被使用0次
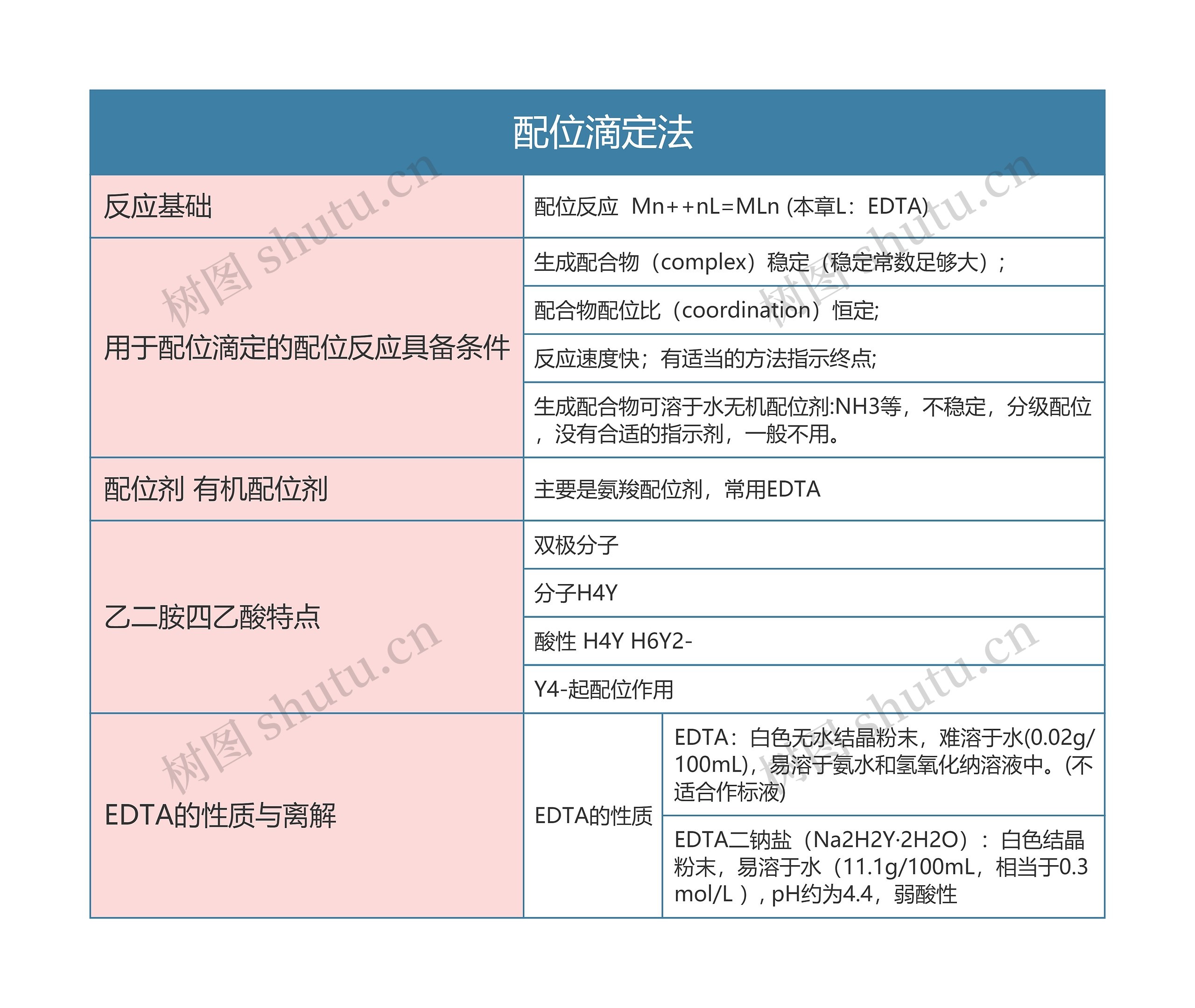
本章节讲述了配位滴定法的知识点,主要内容包括反应基础和EDTA的性质与离解等
树图思维导图提供 分析化学 配位滴定法思维导图 在线思维导图免费制作,点击“编辑”按钮,可对 分析化学 配位滴定法思维导图 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:4d5c6f15a4d80f5eece01167386acbdf
思维导图大纲
配位滴定法思维导图模板大纲
反应基础
配位反应 Mn++nL=MLn (本章L:EDTA)
用于配位滴定的配位反应具备条件
生成配合物(complex)稳定(稳定常数足够大);
配合物配位比(coordination)恒定;
反应速度快;有适当的方法指示终点;
生成配合物可溶于水无机配位剂:NH3等,不稳定,分级配位,没有合适的指示剂,一般不用。
配位剂 有机配位剂
主要是氨羧配位剂,常用EDTA
乙二胺四乙酸特点
双极分子
分子H4Y
酸性 H4Y H6Y2-
Y4-起配位作用
EDTA的性质与离解
EDTA的性质
EDTA:白色无水结晶粉末,难溶于水(0.02g/100mL),易溶于氨水和氢氧化纳溶液中。(不适合作标液)
EDTA二钠盐(Na2H2Y·2H2O):白色结晶粉末,易溶于水(11.1g/100mL,相当于0.3mol/L ), pH约为4.4,弱酸性











 上海工商
上海工商