兽药注册资料要求脑图思维导图

综述,药学研究资料,药理毒理研究资料,临床试验资料等相关内容讲解
树图思维导图提供 兽药注册资料要求脑图 在线思维导图免费制作,点击“编辑”按钮,可对 兽药注册资料要求脑图 进行在线思维导图编辑,本思维导图属于思维导图模板主题,文件编号是:e8ab5e0236be6f0f3763ef445b1b86c6
思维导图大纲
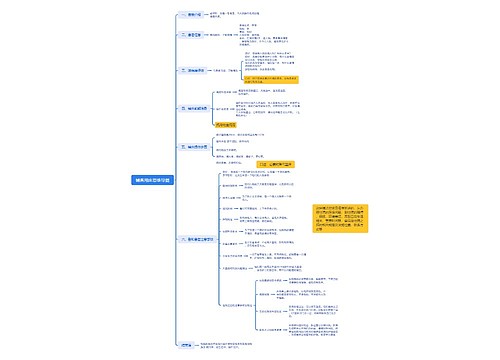
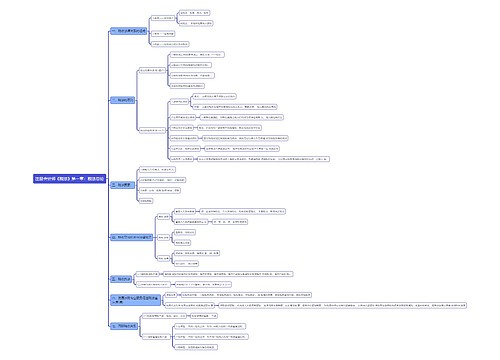
兽药注册资料思维导图模板大纲
(一)综述资料
1.兽药名称
通用名、化学名、英文名、汉语拼音、化学结构式、分子量、分子式。
新制定的名称,应当说明命名依据
2.证明性文件
合法登记证明文件,兽药生产许可证复印件,兽药GMP证书复印件
处方,工艺等专利情况及其权属状态说明,以及对他人专利不构成侵权的保证书
兽药临床试验批准文件
包装材料容器符合药用要求的证明性文件
3.立题目的与依据
国内外有关兽药研发,上市销售现状及相关文献或生产,使用情况综述,复方制剂的组方依据等
4.对主要研究结果的总结及评价
对主要研究结果进行总结,从安全,有效性,质量可控方面对申报品种综合评价
5.兽药说明书样稿、起草说明及最新参考文献
说明书样稿,起草说明及最新参考文献,各项说明的的起草说明,文献
6.包装、标签设计样稿
(二)药学研究资料
7.药学研究资料综述
申请兽药的药学研究(合成工艺、结构确证、剂型选择、处方筛选、质量研究和质量标准制定、稳定性研究等)的试验和国内外文献资料的综述
8.确证化学结构或者组份的试验资料及文献资料
9.原料药生产工艺的研究资料及文献资料
包括工艺流程和化学反应式、起始原料和有机溶媒、反应条件(温度、压力、时间、催化剂等)和操作步骤、精制方法及主要理化常数,并注明投料量和收率以及工艺过程中可能产生或夹杂的杂质或其他中间产物。
10.制剂处方及工艺的研究资料及文献资料;辅料的来源及质量标准
11.质量研究工作的试验资料及文献资料
理化性质、纯度检查、溶出度、含量测定及方法学研究和验证
12.兽药标准草案及起草说明
质量标准应当符合《中国兽药典》现行版的格式,并使用其术语和计量单位。所用试药、试液、缓冲液、滴定液等,应当采用《中国兽药典》现行版收载的品种及浓度,有不同的,应详细说明。兽药标准起草说明应当包括标准中控制项目的选定、方法选择、检查及纯度和限度范围等的制定依据
13.兽药标准品或对照物质的制备及考核材料
提供标准物质或对照物质,并说明其来源、理化常数、纯度、含量及其测定方法和数据
14.药物稳定性研究的试验资料及文献资料
直接接触药物的包装材料和容器共同进行的稳定性试验
15.直接接触兽药的包装材料和容器的选择依据及质量标准
16.样品的检验报告书
申报样品的自检报告,应提供连续3批样品的自检报告
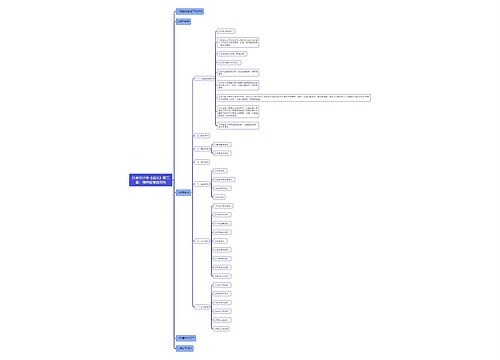
(三)药理毒理研究资料
17.药理毒理研究资料综述
申请兽药的药理毒理研究(包括药效学、作用机制、安全药理、毒理等)的试验和国内外文献资料的综述
18.主要药效学试验资料。(药理研究试验资料及文献资料)
19.安全药理学研究的试验资料及文献资料。
20.微生物敏感性试验资料及文献资料。
申请的兽药为抗感染药物或抗球虫药物时,必须提供抗微生物或抗寄生虫药物对历史和现行临床分离的细菌和寄生虫的敏感性比较研究。
21.药代动力学试验资料及文献资料
22.急性毒性试验资料及文献资料。
23.亚慢性毒性试验资料及文献资料。
24.致突变试验资料及文献资料。
25.生殖毒性试验(含致畸试验)资料及文献资料。
26.慢性毒性(含致癌试验)资料及文献资料。
27.过敏性(局部、全身和光敏毒性)、溶血性和局部(血管、皮肤、粘膜、肌肉等)刺激性等主要与局部、全身给药相关的特殊安全性试验资料。
(四)临床试验资料
28.国内外相关的临床试验资料综述
国内外有关该品种临床研究的文献、摘要及近期追踪报道的综述
29.临床试验批准文件,试验方案、临床试验资料
30.靶动物安全性试验资料
(五)残留试验资料
31.国内外残留试验资料综述
指研究申请的兽药或代谢物在给药动物组织是否产生残留,残留的程度和残留时间。该资料应说明兽药的残留标识物,残留靶组织,每日允许摄入量,最高残留限量,残留检测方法和休药期等
32.残留检测方法及文献资料
33.残留消除试验研究资料,包括试验方案
通过研究申请的兽药在靶动物的体内消除过程,以确定是否在推荐的使用条件下在给药的动物组织中是否产生残留,并确定需要遵守的休药期。用于动物微生物或寄生虫感染的药物还应提供残留物对人肠道菌群丛的潜在作用,评价对食品加工业的影响。
(六)生态毒性试验资料
34.生态毒性试验资料及文献资料
是指通过研究申请的兽药在靶动物体内的代谢和排泄情况,研究排出体外的兽药及代谢物在环境中的各种降解途径,对环境潜在的影响,并提出为减少这种影响而需要采取的必要预防措施。同时还需要提供盛装药物的容器、未使用完的药物或废弃物对环境、水生生物、植物和其它非靶动物的影响和有效的处理方法










 上海工商
上海工商